题目内容
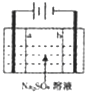 近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产模根,下列主产法中不正确的是( )
近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产模根,下列主产法中不正确的是( )| A、阴极反应式4OH--4e-=2H2O+O2↑ |
| B、阴极得到NaOH,阳极得到H2SO4 |
| C、每生产1molH2SO4,同时得到2mol NaOH |
| D、此反应实质就是电解水 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电解硫酸钠溶液时,阳极上水失电子生成氧气同时生成氢离子,所以阳极区域还生成硫酸,阴极上水得电子生成氢气同时生成氢氧根离子,阴极区域生成NaOH,实质上仍然是电解水,据此分析解答.
解答:
解:电解硫酸钠溶液时,阳极上水失电子生成氧气同时生成氢离子,所以阳极区域还生成硫酸,阴极上水得电子生成氢气同时生成氢氧根离子,阴极区域生成NaOH,实质上仍然是电解水,
A.阴极反应式2H2O+2e-=2HO-+H2↑,故A错误;
B.通过以上分析知,阴极得到NaOH,阳极得到H2SO4,故B正确;
C.阴极反应式4H2O+4e-=4HO-+2H2↑,阳极反应式为2H2O-4e-=4H++O2↑,在得失电子相同条件下,每生产1molH2SO4,同时得到2molNaOH,故C正确;
D.阳极上生成氧气、阴极上生成氢气,所以实质上是电解水,故D正确;
故选A.
A.阴极反应式2H2O+2e-=2HO-+H2↑,故A错误;
B.通过以上分析知,阴极得到NaOH,阳极得到H2SO4,故B正确;
C.阴极反应式4H2O+4e-=4HO-+2H2↑,阳极反应式为2H2O-4e-=4H++O2↑,在得失电子相同条件下,每生产1molH2SO4,同时得到2molNaOH,故C正确;
D.阳极上生成氧气、阴极上生成氢气,所以实质上是电解水,故D正确;
故选A.
点评:本题考查电解原理,侧重考查分析能力,明确各个电极上发生的反应是解本题关键,会正确书写电极反应式,题目难度不大.

练习册系列答案
相关题目
下列过程中发生取代反应的是( )
| A、乙烯通往Br2的CCl4溶液中生成1,2---二溴乙烷 |
| B、乙醇在空气中燃烧生成CO2和H2O |
| C、用氯乙烯制聚氯乙烯 |
| D、甲烷与氯气混合后光照生成一氯甲烷 |
关于溶液中微粒的浓度,下列说法正确的是( )
| A、0.1mol?L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | ||
| B、等浓度等体积的NaHSO3溶液与NaClO溶液混合后:c(Na+)+c(H+)=c(HSO3-)+c(ClO-)+2c(SO32-)+c(OH-) | ||
C、等浓度等体积的NaHCO3溶液与NaCl溶液混合后:
| ||
| D、标况下,将2.24L SO2气体通入到100ml 1mol?L-1的NaOH溶液中,完全反应后溶液呈酸性,则该溶液中:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) |
利用电解原理,在铁皮表面镀一层锌的有关叙述正确的是( )
| A、铁为负极,锌为正极 |
| B、铁为阳极,锌为阴极 |
| C、用可溶性铁盐作电解液 |
| D、锌元素既被氧化又被还原 |
下列关于化学平衡常数的说法中,正确的是( )
| A、在任何条件下,化学平衡常数K都是一个定值 |
| B、当改变反应物的浓度时,化学平衡常数会发生改变 |
| C、化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 |
| D、化学平衡常数K与反应物的转化率是一一对应的 |
下列有关铜锌原电池的叙述正确的是( )
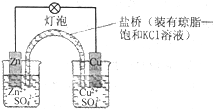

| A、盐桥中的Cl-移向CuSO4溶液 |
| B、电池总反应为Zn+Cu2+=Zn2++Cu |
| C、在外电路中,电子从正极流向负极 |
| D、取下盐桥,原电池仍可工作 |
下列物质中,含有的分子数目最少的是( )
| A、0.5molCO2 |
| B、标准状况下11.2L氨气 |
| C、8 g水 |
| D、6.02×1023个氯分子 |
