题目内容
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )| A、元素Q的非金属性比R的强 |
| B、离子半径的大小顺序:r(Tm+)>r(Wn-) |
| C、元素Q的氧化物均为酸性氧化物 |
| D、元素T与元素R的最高正价之和等于8 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素Q、R、T、W在元素周期表中的位置,可知Q、R处于第二周期,T、W处于第三周期,T所处的周期序数与主族序数相等,则T为Al,可推知Q为C元素、R为N元素、W为S元素.
A.同周期自左而右非金属性增强;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
C.CO不是酸性氧化物;
D.Al元素最高正化合价为+3,N元素最高正化合价为+5.
A.同周期自左而右非金属性增强;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
C.CO不是酸性氧化物;
D.Al元素最高正化合价为+3,N元素最高正化合价为+5.
解答:
解:由短周期元素Q、R、T、W在元素周期表中的位置,可知Q、R处于第二周期,T、W处于第三周期,T所处的周期序数与主族序数相等,则T为Al,可推知Q为C元素、R为N元素、W为S元素.
A.同周期自左而右非金属性增强,故非金属性N>C,故A错误;
B.Al3+离子比S2-离子少一个电子层,故离子半径:r(Al3+)<r(S2-),故B错误;
C.CO是不成盐氧化物,不是酸性氧化物,故C错误;
D.Al元素最高正化合价为+3,N元素最高正化合价为+5,二者最高正价之和等于8,故D正确,
故选D.
A.同周期自左而右非金属性增强,故非金属性N>C,故A错误;
B.Al3+离子比S2-离子少一个电子层,故离子半径:r(Al3+)<r(S2-),故B错误;
C.CO是不成盐氧化物,不是酸性氧化物,故C错误;
D.Al元素最高正化合价为+3,N元素最高正化合价为+5,二者最高正价之和等于8,故D正确,
故选D.
点评:本题考查结构性质位置关系应用,难度不大,注意掌握金属性、非金属性强弱比较及微粒半径比较.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
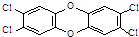 1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是
1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是( )
| A、它的分子式为C12H4O2Cl4 |
| B、它不能发生加成反应 |
| C、它的一溴取代物有一种 |
| D、此分子中共平面的原子最多有22个 |
某反应的△H=-80kJ?mol-1,叙述正确的是( )
| A、正反应活化能等于80kJ?mol-1 |
| B、逆反应活化能一定大于80kJ?mol-1 |
| C、逆反应活化能不大于80kJ?mol-1 |
| D、正反应活化能比逆反应活化能小80kJ?mol-1 |
化学与生活息息相关,下列说法正确的是( )
| A、HClO是弱酸,所以NaClO是弱电解质 |
| B、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C、放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 |
| D、自来水水阀生锈主要是化学腐蚀所致 |
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1mol硝基(-NO2)与NA个二氧化氮气体分子所含电子数相等 |
| B、1mol氢氧根离子(OH-)与NA个羟基(-OH)所含电子数相等 |
| C、在相同温度下,pH=1且体积为1L的硫酸溶液所含氢离子数与pH=13且体积为1L的氢氧化钠溶液所含氢氧根离子数一定均为0.1NA |
| D、在反应2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑中,每生成1molO2该反应共转移的电子数为6NA |
下列一定能说明酸HX是弱电解质的是( )
①常温下NaX溶液的pH大于7;
②HX溶液做导电实验,灯泡很暗;
③HX不与NaCl反应;
④0.1mol/L的HX溶液的pH=2;
⑤HX具有很强的挥发性;
⑥pH=1的HX加水稀释成10倍后,pH=1.5.
①常温下NaX溶液的pH大于7;
②HX溶液做导电实验,灯泡很暗;
③HX不与NaCl反应;
④0.1mol/L的HX溶液的pH=2;
⑤HX具有很强的挥发性;
⑥pH=1的HX加水稀释成10倍后,pH=1.5.
| A、②③⑤ | B、①④⑥ |
| C、①②④⑥ | D、①②③④⑤⑥ |
某有机物的结构简式为: ,下列对其性质的叙述中不正确的是( )
,下列对其性质的叙述中不正确的是( )
 ,下列对其性质的叙述中不正确的是( )
,下列对其性质的叙述中不正确的是( )| A、不能与钠反应放出氢气 |
| B、能与溴水发生加成反应 |
| C、能发生加聚反应 |
| D、不能与新制的Cu(OH)2悬浊液反应 |
下列关于晶体的说法一定正确的是( )
| A、第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴阳离子排列方式相同 |
| B、晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子 |
| C、离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键 |
D、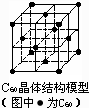 C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个 |
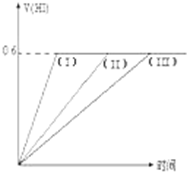 在一定温度下发生反应:I2(g)+H2(g)?2HI(g);并达平衡.HI的体积分数V(HI)%随时间变化如图曲线(II)所示.若改变反应条件,在甲条件下的变化如曲线(I)所示.在乙条件下的变化如曲线(III)所示.则甲条件、乙条件分别是( )
在一定温度下发生反应:I2(g)+H2(g)?2HI(g);并达平衡.HI的体积分数V(HI)%随时间变化如图曲线(II)所示.若改变反应条件,在甲条件下的变化如曲线(I)所示.在乙条件下的变化如曲线(III)所示.则甲条件、乙条件分别是( )