题目内容
下列关于晶体的说法一定正确的是( )
| A、第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴阳离子排列方式相同 |
| B、晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子 |
| C、离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键 |
D、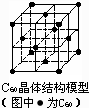 C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个 |
考点:离子晶体,晶胞的计算
专题:化学键与晶体结构
分析:A、氯化钠晶胞中阴阳离子的配位数为6而氯化铯晶胞中阴阳离子的配位数为8,所以晶体中阴阳离子排列方式不同,据此判断;
B、在金属晶体中只有自由电子和阳离子,没有阴离子,据此判断;
C、离子晶体中有离子键也可以有共价键,有的分子晶体中没有共价键,例如单原子分子形成的晶体,据此判断;
D、以晶胞顶点上的C60为例,与之距离最近的分子在经过该点的面的面心上,这样的面有12个,所以这样的分子也有12个,据此判断.
B、在金属晶体中只有自由电子和阳离子,没有阴离子,据此判断;
C、离子晶体中有离子键也可以有共价键,有的分子晶体中没有共价键,例如单原子分子形成的晶体,据此判断;
D、以晶胞顶点上的C60为例,与之距离最近的分子在经过该点的面的面心上,这样的面有12个,所以这样的分子也有12个,据此判断.
解答:
解:A、氯化钠晶胞中阴阳离子的配位数为6而氯化铯晶胞中阴阳离子的配位数为8,所以晶体中阴阳离子排列方式不同,故A错误;
B、在金属晶体中只有自由电子和阳离子,没有阴离子,故B错误;
C、离子晶体中有离子键可能有共价键,有的分子晶体中没有共价键,例如单原子分子形成的晶体,故C错误;
D、以晶胞顶点上的C60为例,与之距离最近的分子在经过该点的面的面心上,这样的面有12个,所以这样的分子也有12个,故D正确;
故选D.
B、在金属晶体中只有自由电子和阳离子,没有阴离子,故B错误;
C、离子晶体中有离子键可能有共价键,有的分子晶体中没有共价键,例如单原子分子形成的晶体,故C错误;
D、以晶胞顶点上的C60为例,与之距离最近的分子在经过该点的面的面心上,这样的面有12个,所以这样的分子也有12个,故D正确;
故选D.
点评:本题主要考查晶胞结构,难度不大,在解题时要注意不能思维定势,要仔细审题.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
已知w g物质A在O2中充分燃烧后,产物被足量的Na2O2完全吸收后,Na2O2固体增重w g,当A为H2或CO时,上述说法成立.据此推断A不可能是下列物质中的( )
| A、H2和CO的混合气 |
| B、D2 |
| C、甲醇 |
| D、乙醇 |
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )| A、元素Q的非金属性比R的强 |
| B、离子半径的大小顺序:r(Tm+)>r(Wn-) |
| C、元素Q的氧化物均为酸性氧化物 |
| D、元素T与元素R的最高正价之和等于8 |
下列实验不能达到目的是( )
A、 测定一定时间内生成H2的反应速率 |
B、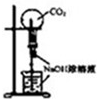 用CO2作喷泉实验 |
C、 验证NH3易溶于水实验 |
D、 测定酸碱中和反应的中和热 |
下列各化合物的命名中不正确的是( )
| A、CH2=CH-CH=CH2 1,3-丁二烯 |
B、 3-丁醇 3-丁醇 |
C、 邻-甲基苯酚 邻-甲基苯酚 |
D、 2-甲基丁烷 2-甲基丁烷 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、在1 L 0.2 mol?L-1的Na2CO3溶液中含有CO32-的数目为0.2NA |
| B、0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA |
| C、15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.2NA |
| D、1 mol Na2O2中含有的阴离子数目为2NA |
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m、分子式为C32H16N8Co)恢复了磁性.已知该物质主要用于有机反应中的催化剂以及光电子等高新技术领域.下列说法中不正确的是( )
| A、“钴酞菁”分子所形成的分散系具有丁达尔效应 |
| B、该物质属于有机高分子化合物 |
| C、此项工作的研究表明,人们可以改变分子的某些物理性质 |
| D、此项研究结果可广泛应用于光电器件、生物技术等方面 |
下列说法不正确的是( )
| A、利用丁达尔现象可以鉴别胶体和溶液 |
| B、在豆浆里加入盐卤做豆腐与胶体的聚沉有关 |
| C、胶体与溶液的分离可用渗析的方法 |
| D、KCl溶液、淀粉溶液和纯水都属于分散系 |
 下列有关实验没有明显错误的是( )
下列有关实验没有明显错误的是( )| A、使用湿润过的pH试纸测量某溶液的pH |
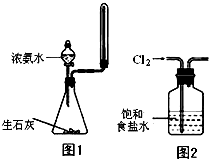
| B、实验室可以用图1所示装置来制取少量氨气 |
| C、用量筒量取20 mL 0.50mol?L-1H2SO4溶液于烧杯中,加水80 mL,配制成0.10mol?L-1H2SO4溶液 |
| D、实验室用图2所示装置除去Cl2中的少量HCl |