题目内容
短周期元素X、Y、Z组成的化合物Y2X和ZX2,Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3,已知三种元素原子的电子总数为25,且Z和Y的原子序数之和比X的原子序数的2倍还多1,Z原子的最外层电子数是次外层电子数的2倍.请回答下列问题:
(1)写出X、Y、Z的元素符号:
X: Y: Z:
(2)写出ZX2的化学式
(3)Y2X对应水化物的电子式为 ,该水化物中含有的化学键有 (填化学键类型)
(1)写出X、Y、Z的元素符号:
X:
(2)写出ZX2的化学式
(3)Y2X对应水化物的电子式为
考点:位置结构性质的相互关系应用
专题:
分析:由Z原子的最外层电子数是次外层电子数的2倍,则Z为两个电子层时,推出Z为碳元素,
再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,则设X原子的质子数为x,Y原子的质子数为y,根据题意,可得出以下关系:
解得:x=8,y=11,即X为氧元素,Y为钠元素,然后利用单质及化合物的性质来解答.
再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,则设X原子的质子数为x,Y原子的质子数为y,根据题意,可得出以下关系:
|
解得:x=8,y=11,即X为氧元素,Y为钠元素,然后利用单质及化合物的性质来解答.
解答:
解:由Z原子的最外层电子数是次外层电子数的2倍,则Z为两个电子层时,推出Z为碳元素,
再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,则设X原子的质子数为x,Y原子的质子数为y,根据题意,可得出以下关系:
解得:x=8,y=11,即X为氧元素,Y为钠元素,
(1)X为氧元素(O),Y为钠元素(Na),Z为碳元素(C),故答案为:O;Na;C;
(2)X为氧元素(O),Z为碳元素(C),ZX2的化学式为CO2,故答案为:CO2;
(3)化合物Y2X对应的水化物为NaOH,其电子式为 ,存在的化学键有离子键和共价键,
,存在的化学键有离子键和共价键,
故答案为: ;离子键和共价键.
;离子键和共价键.
再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,则设X原子的质子数为x,Y原子的质子数为y,根据题意,可得出以下关系:
|
解得:x=8,y=11,即X为氧元素,Y为钠元素,
(1)X为氧元素(O),Y为钠元素(Na),Z为碳元素(C),故答案为:O;Na;C;
(2)X为氧元素(O),Z为碳元素(C),ZX2的化学式为CO2,故答案为:CO2;
(3)化合物Y2X对应的水化物为NaOH,其电子式为
 ,存在的化学键有离子键和共价键,
,存在的化学键有离子键和共价键,故答案为:
 ;离子键和共价键.
;离子键和共价键.
点评:本题考查位置、结构、性质的关系,为高频考点,侧重于学生的分析能力的考查,学生熟悉有关原子的核外电子排布、原子序数与质子数的关系、电子式、化学键及物质的性质等方面的知识是解答本题的关键,难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
下列方程式书写正确的是( )
| A、HCO3-在水溶液中的电离方程式:HCO3-+H2O?H3O++CO32- |
| B、H2SO3的电离方程式H2SO3?2H++SO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、CuSO4的水解方程式:Cu2++2H2O?Cu(OH)2+2H+ |
A、B、C短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,现有以下说法,判断正确的是( )
| A | B |
| C |
| A、B形成的单质存在同素异形体,C的单质不存在同素异形体 |
| B、C的最高价氧化物对应的水化物能与A的常见氢化物形成三种盐 |
| C、常温下,B的氢化物中无H+ |
| D、Y的种类比X多 |
实验是化学研究的基础.下列实验能达到实验目的是( )
A、 石油的分馏 |
B、 分离硝基苯和水 |
C、 除去甲烷中的乙烯 |
D、 制取并收集乙炔气体 |
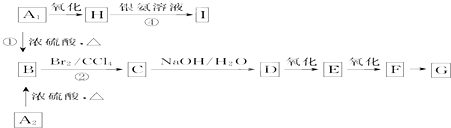
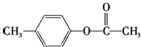 、
、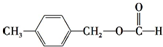 外,其余的结构简式为
外,其余的结构简式为