题目内容
现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图 .
(2)写出Y元素最高价氧化物的水化物分别与HCl、NaOH溶液反应的离子反应方程式 、 .
(3)写出X与Y的电子排布式 、 .
(4)元素T与氯元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 .
A.气态氢化物的挥发性和稳定性
B.两元素的电负性
C.含氧酸的酸性
D.氢化物中X-H键的键长(X代表T和Cl两元素)
E、两元素在自然界的存在形态.
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(2)写出Y元素最高价氧化物的水化物分别与HCl、NaOH溶液反应的离子反应方程式
(3)写出X与Y的电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性
B.两元素的电负性
C.含氧酸的酸性
D.氢化物中X-H键的键长(X代表T和Cl两元素)
E、两元素在自然界的存在形态.
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:在短周期元素中,单质能与水剧烈反应,所得溶液呈弱酸性,则T为F元素,X的L层p电子数比s电子数多2个,核外电子排布为1s22s22p4,则X为O元素,第三周期元素的简单离子中半径最小的离子为Al3+,则Y为Al元素,Z的L层有三个未成对电子,核外电子排布为1s22s22p3,则Z为N元素,以此解答该题.
解答:
解:在短周期元素中,单质能与水剧烈反应,所得溶液呈弱酸性,则T为F元素,X的L层p电子数比s电子数多2个,核外电子排布为1s22s22p4,则X为O元素,第三周期元素的简单离子中半径最小的离子为Al 3+,则Y为Al元素,Z的L层有三个未成对电子,核外电子排布为1s22s22p3,则Z为N元素,
(1)X为氧元素,它的离子结构示意图为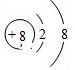 ,故答案为:
,故答案为: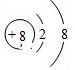 ;
;
(2)Y元素最高价氧化物的水化物为氢氧化铝,分别与HCl、NaOH溶液反应的离子反应方程式为Al(OH)3+3H+═Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+3H+═Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)氧的电子排布式为1s22s22p4,铝的电子排布式为1s22s22p63s23p1,
故答案为:1s22s22p4;1s22s22p63s23p1;
(4)F的非金属性比Cl元素强,可根据得电子能力判断,能证明这一事实的是,
A.气态氢化物的挥发性和稳定性与得失电子能力无关,故错误;
B.根据两元素的电负性可判断得失电子能力,故正确;
C.根据元素周期律,非金属性越强,含氧酸的酸性就越强,故正确;
D.氢化物中X-H键的键长越长,说明氢化物越不稳定,根据元素周期律,可知,非金属必越弱,故正确;
E、两元素在自然界中都是以化合态的形态存在,故无法判断得失电子能力,故错误;
故答案为:F;BD.
(1)X为氧元素,它的离子结构示意图为
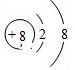 ,故答案为:
,故答案为: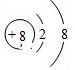 ;
;(2)Y元素最高价氧化物的水化物为氢氧化铝,分别与HCl、NaOH溶液反应的离子反应方程式为Al(OH)3+3H+═Al3++3H2O、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+3H+═Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)氧的电子排布式为1s22s22p4,铝的电子排布式为1s22s22p63s23p1,
故答案为:1s22s22p4;1s22s22p63s23p1;
(4)F的非金属性比Cl元素强,可根据得电子能力判断,能证明这一事实的是,
A.气态氢化物的挥发性和稳定性与得失电子能力无关,故错误;
B.根据两元素的电负性可判断得失电子能力,故正确;
C.根据元素周期律,非金属性越强,含氧酸的酸性就越强,故正确;
D.氢化物中X-H键的键长越长,说明氢化物越不稳定,根据元素周期律,可知,非金属必越弱,故正确;
E、两元素在自然界中都是以化合态的形态存在,故无法判断得失电子能力,故错误;
故答案为:F;BD.
点评:本题主要考查了结构示意图、电子排布式、元素周期律、常见元素化合物知识,中等难度,解题的关键在于元素推断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知X、Y、Z、W、T是短周期中原子序数依次增大的5种主族元素.其中Y和X两种元素可以组成1:1、1:2、1:3、1:4等多种化合物; Z原子最外层电子数是次外层电子数的3倍,W与X同主族,W与T形成的化合物WT是厨房必需的调味品.下列说法正确的是( )
| A、原子半径:T>W>Z>Y |
| B、W与T的单质可通过电解饱和的WT水溶液获得 |
| C、Z与W形成的两种化合物中化学键类型完全相同 |
| D、元素X、Z与T可形成多种酸 |
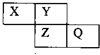 X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )
X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )| A、X与Q的化合物中不含有共价键 |
| B、最高价氧化物对应水化物的酸性:Q比Z强 |
| C、氢化物稳定性:Y比Z强 |
| D、Q与Fe反应生成的化合物中,铁元素显+3价 |
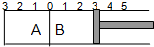 如图所示,温度不变的某容器分隔成A、B两部分,A容器容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2(g)+O2(g)?2SO3(g),
如图所示,温度不变的某容器分隔成A、B两部分,A容器容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2(g)+O2(g)?2SO3(g),