题目内容
下列方程式书写正确的是( )
| A、HCO3-在水溶液中的电离方程式:HCO3-+H2O?H3O++CO32- |
| B、H2SO3的电离方程式H2SO3?2H++SO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、CuSO4的水解方程式:Cu2++2H2O?Cu(OH)2+2H+ |
考点:离子方程式的书写
专题:
分析:A.碳酸氢根离子为多元弱酸酸式根离子,电离生成氢离子和碳酸根离子;
B.亚硫酸为多元弱酸,分步电离;
C.碳酸根离子水解分两步,以第一步为主;
D.硫酸铜为弱碱强酸盐,水解生成氢氧化铜和硫酸.
B.亚硫酸为多元弱酸,分步电离;
C.碳酸根离子水解分两步,以第一步为主;
D.硫酸铜为弱碱强酸盐,水解生成氢氧化铜和硫酸.
解答:
解:A.碳酸氢根离子为多元弱酸酸式根离子,电离生成氢离子和碳酸根离子,电离方程式为:HCO3-+H2O?H3O++CO32-,故A正确;
B.亚硫酸为多元弱酸,分步电离,电离方程式为:H2SO3? H++HSO3-,HSO3-?
H++HSO3-,HSO3-? H++SO32-,故B错误;
H++SO32-,故B错误;
C.碳酸根离子水解分两步,以第一步为主,CO32-的水解方程式:CO32-+H2O? HCO3-+OH-,故C错误;
HCO3-+OH-,故C错误;
D.硫酸铜为弱碱强酸盐,水解生成氢氧化铜和硫酸,水解离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,故D正确;
故选:AD.
B.亚硫酸为多元弱酸,分步电离,电离方程式为:H2SO3?
 H++HSO3-,HSO3-?
H++HSO3-,HSO3-? H++SO32-,故B错误;
H++SO32-,故B错误;C.碳酸根离子水解分两步,以第一步为主,CO32-的水解方程式:CO32-+H2O?
 HCO3-+OH-,故C错误;
HCO3-+OH-,故C错误;D.硫酸铜为弱碱强酸盐,水解生成氢氧化铜和硫酸,水解离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,故D正确;
故选:AD.
点评:本题考查了离子方程式是书写,侧重考查盐类的水解和电解质的电离方程式,明确电解质强弱及电离的方式和盐类水解的规律是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质属于苯的同系物的是( )
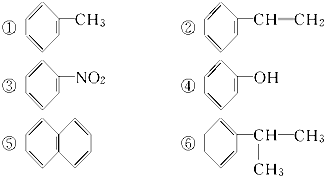

| A、①⑥ | B、①②⑤⑥ |
| C、①②⑥ | D、②③④⑤⑥ |
血液化验单中“葡萄糖”一项的结果为4.94×10-3 mol?L-1.这里的“4.94×10-3 mol?L-1”表示葡萄糖的( )
| A、物质的量 | B、摩尔质量 |
| C、质量分数 | D、物质的量浓度 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、4℃时9mL水和标准状况下11.2L氮气含有相同的原子数 |
| B、27g金属铝与足量的盐酸反应时,失去的电子数为2NA |
| C、常温常压下,48gO3含有的氧原子数为3NA |
| D、5.6gC2H4和C4H8混合气中含氢原子数为0.6 NA |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、羟基的电子式: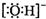 |
C、甲烷分子的比例模型: |
D、乙醇的结构式: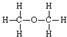 |