题目内容
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙的气态化合物的水溶液呈碱性,甲与丙同主族,丁元素原子最外层电子数与其电子层数相等.下列说法正确的是( )
| A、原子半径:丁>丙>甲 |
| B、单质的还原性:丁>丙>甲 |
| C、甲、乙、丙的氧化物为共价化合物 |
| D、乙、丙、丁的最高价氧化物对应的水化物相互反应 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素甲、乙、丙丁、的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,则甲为H,乙为N;甲和丙同主族,原子序数大于N,则丙为Na;丁元素原子最外层电子数与其电子层数相等,则丁在第三周期第ⅢA族,即丁为Al,以此来解答.
解答:
解:短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,则甲为H,乙为N;甲和丙同主族,原子序数大于N,则丙为Na;丁元素原子最外层电子数与其电子层数相等,则丁在第三周期第ⅢA族,即丁为Al,
A.同周期原子半径从左向右减小,电子层越多原子半径越大,则原子半径:丙>丁>甲,故A错误;
B.金属性越强,单质的还原性越强,则单质的还原性:丙>丁>甲,故B错误;
C.甲、乙的氧化物为共价化合物,丙的氧化物为离子化合物,故C错误;
D.乙、丙、丁的最高价氧化物对应的水化物分别为硝酸、氢氧化钠、氢氧化铝,氢氧化铝为两性氢氧化物,能与硝酸、氢氧化钠反应,硝酸与氢氧化钠发生中和反应,故D正确;
故选D.
A.同周期原子半径从左向右减小,电子层越多原子半径越大,则原子半径:丙>丁>甲,故A错误;
B.金属性越强,单质的还原性越强,则单质的还原性:丙>丁>甲,故B错误;
C.甲、乙的氧化物为共价化合物,丙的氧化物为离子化合物,故C错误;
D.乙、丙、丁的最高价氧化物对应的水化物分别为硝酸、氢氧化钠、氢氧化铝,氢氧化铝为两性氢氧化物,能与硝酸、氢氧化钠反应,硝酸与氢氧化钠发生中和反应,故D正确;
故选D.
点评:本题考查结构性质位置关系应用,涉及元素周期律、元素化合物的性质,推断元素是解答本题的关键,注意氨气的水溶液为碱性是推断突破口,难度不大.

练习册系列答案
相关题目
向明矾溶液中逐渐滴加Ba(OH)2溶液,符合要求的离子方程式为( )
| A、加入过量的Ba(OH)2溶液时:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓ |
| B、溶液恰好呈中性时:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C、SO42-离子恰好完全沉淀时:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D、明矾与Ba(OH)2按物质的量比1:1反应时:Al3++SO42-+Ba2++3OH-→Al(OH)3↓+BaSO4↓ |
在pH=l的溶液中,能大量共存的一组离子或分子是( )
| A、Mg2+、Ca2+、ClO-、NO-3 |
| B、Na+、K+、SiO2-3、Cl- |
| C、K+、Cr2O2-7、CH3CHO、SO2-4 |
| D、Al3+、NH+4、Br-、Cl- |
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A、H2O2 |
| B、IO3- |
| C、MnO4- |
| D、HNO2 |
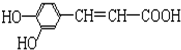
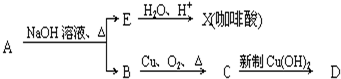
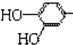 结构;②能发生水解反应;R的结构简式为
结构;②能发生水解反应;R的结构简式为
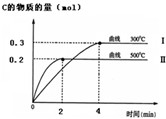 (1)已知在25℃时:①2CO (s)+O2(g)═2CO2(g)△H1=-566KJ/mol
(1)已知在25℃时:①2CO (s)+O2(g)═2CO2(g)△H1=-566KJ/mol