籾朕坪否
厮岑和双蛍徨賜宣徨壓磨來訳周和脅嬬剳晒KI⇧徭附窟伏泌和延晒⦿H2O2★H2O IO3-★I2 MnO4-★Mn2+ HNO2★NO泌惚蛍艶喘吉麗嵎議楚議宸乂麗嵎剳晒怎楚議KI⇧誼欺I2恷謹議頁↙ ⇄
| A、H2O2 |
| B、IO3- |
| C、MnO4- |
| D、HNO2 |
深泣⦿剳晒珊圻郡哘議柴麻,剳晒珊圻郡哘
廨籾⦿窮晒僥廨籾
蛍裂⦿郡哘嶄I-★I2⇧払肇1倖窮徨⇧遇H2O2★H2O誼欺2倖窮徨⇧IO3-★I2誼欺5倖窮徨⇧MnO4-★Mn2+誼欺5倖窮徨⇧HNO2★NO誼欺1倖窮徨⇧功象剳晒珊圻郡哘剳晒質嚥珊圻質誼払窮徨方朕屢吉序佩登僅⤴
盾基⦿
盾⦿剳晒扮I-⇧H2O2★H2O誼欺2倖窮徨⇧IO3-★I2誼欺5倖窮徨⇧MnO4-★Mn2+誼欺5倖窮徨⇧HNO2★NO誼欺1倖窮徨⇧I-★I2⇧払肇1倖窮徨⇧徽喇噐IO3-匆瓜珊圻葎I2⇧夸誼欺I2恷謹議頁IO3-⇧
絞僉B⤴
絞僉B⤴
泣得⦿云籾深臥剳晒珊圻郡哘議柴麻⇧葎互撞深泣⇧廣吭委燐圷殆晒栽勺議延晒⇧IO3-喇噐匆瓜珊圻葎I2葎云籾議叟危泣⇧籾朕佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
玉巓豚圷殆遮、厰、央、供議圻徨會方卆肝奐寄⇧遮才厰議賑蓑晒栽麗議邦卑匣格珠來⇧遮嚥央揖麼怛⇧供圷殆圻徨恷翌蚊窮徨方嚥凪窮徨蚊方屢吉⤴和双傍隈屎鳩議頁↙ ⇄
| A、圻徨磯抄⦿供﹅央﹅遮 |
| B、汽嵎議珊圻來⦿供﹅央﹅遮 |
| C、遮、厰、央議剳晒麗葎慌勺晒栽麗 |
| D、厰、央、供議恷互勺剳晒麗斤哘議邦晒麗屢札郡哘 |
夕嵆頁匯嶽酒準燕幣晒僥延晒狛殻議圭隈⇧和双屢購郡哘議夕嵆嶄危列議頁↙ ⇄
A、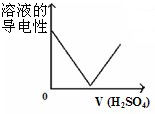 繍匯協楚蓮葬磨砧秘欺揖敵業議Ba↙OH⇄2卑匣嶄 繍匯協楚蓮葬磨砧秘欺揖敵業議Ba↙OH⇄2卑匣嶄 |
B、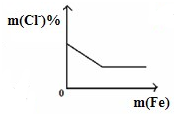 繍鑓頚紗秘欺匯協楚FeCl3卑匣嶄 繍鑓頚紗秘欺匯協楚FeCl3卑匣嶄 |
C、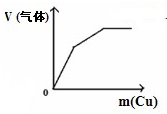 繍有頚紗秘欺匯協楚敵嵓磨嶄 繍有頚紗秘欺匯協楚敵嵓磨嶄 |
D、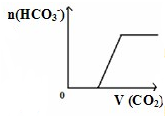 繍屈剳晒娘宥秘欺匯協楚働頚娼卑匣嶄 繍屈剳晒娘宥秘欺匯協楚働頚娼卑匣嶄 |
64g有嚥匯協敵業議嵓磨郡哘⇧有頼畠卑盾⇧伏撹NO才NO2↙音深打伏撹N2O4⇄詞栽賑悶33.6L↙侭嗤賑悶悶持譲壓炎彈彜趨和霞誼⇄⤴和双傍隈屎鳩議頁↙ ⇄
| A、恢伏議NO壓炎彈彜趨和議悶持葎28L |
| B、歌紗郡哘議嵓磨議麗嵎議楚葎1.5mol |
| C、NO才NO2議麗嵎議楚岻曳葎1⦿5 |
| D、飛伏撹議賑悶頼畠瓜邦簾辺⇧俶勣炎彈彜趨和O2議悶持葎 22.4L |