题目内容
12.下列各组反应中,最后得到Al(OH)3沉淀的是( )| A. | 将Al2O3固体粉末加到沸水中 | |
| B. | 将CO2气体不断通人到NaAlO2溶液中 | |
| C. | 将过量的金属钠投入到NaAlO2溶液中 | |
| D. | 向340ml 1mol/L NaOH溶液中加入80ml 1mol/L的AlCl3溶液 |
分析 A.Al2O3与水不反应;
B.碳酸酸性比氢氧化铝强,过量CO2通入NaAlO2溶液中生成氢氧化铝白色沉淀;
C.钠和水反应生成氢氧化钠;
D.n(NaOH)=0.34mol,n(AlCl3)=0.08mol,结合反应的离子方程式判断.
解答 解:A.Al2O3不溶于热水中,与水不反应,故A错误;
B.碳酸酸性比氢氧化铝强,过量CO2通入NaAlO2溶液中生成氢氧化铝白色沉淀,故B正确;
C.金属钠投入到NaAlO2,发生的反应为:2Na+2H2O=2NaOH+H2 ↑,没有生成Al(OH)3,故C错误;
D.n(NaOH)=0.34mol,n(AlCl3)=0.08mol,分别发生3OH+Al3+=Al(OH)3↓,AlOH3+OH-=AlO2-+2H2O,所以最终没有沉淀生成,故D错误.
故选B.
点评 本题考查物质之间的化学反应,为高频考点,熟悉复分解反应发生的条件及常见物质的溶解性是解答本题的关键,注意D为易错选项,高频考题,题目难度中等.

练习册系列答案
相关题目
13.A、B、C、D四种物质之间的转化关系如图所示(部分产物略去),下列说法正确的是( )
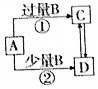

| A. | 若A为AlCl3溶液,B 可能为氨水,反应①的离子方程式为Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 若A为Fe,B可能为稀HNO3,反应②的离子方程式为3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| C. | 若A为NaOH溶液,B可能为CO2,可用Ca(OH)2溶液鉴定C、D 溶液中的阴离子 | |
| D. | 若A为Cl2,B可能为NH3,实验室可用加热固体C的方法制取NH3 |
3.下列无色气体中,遇空气变成红棕色的是( )
| A. | CO | B. | HCl | C. | SO2 | D. | NO |
4.同温同压下,甲乙两容器分别装有CH4和NH3气体,已知它们所含原子数相同,则甲乙两容器体积比为( )
| A. | 4:3 | B. | 4:5 | C. | 5:4 | D. | 1:1 |
1.0.5L 2mol/L FeCl3溶液与0.2L 5mol/L KCl溶液中的Cl-物质的量之比( )
| A. | 6:5 | B. | 3:2 | C. | 15:2 | D. | 3:1 |
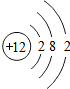 ,其电子所占据的电子层中,能量最高的是M层(填符号).
,其电子所占据的电子层中,能量最高的是M层(填符号).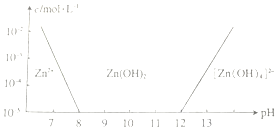 锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.
锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.