��Ŀ����
20����֪����Ԫ�ص����ʻ�ԭ�ӽṹ��������������ʾ���ش��������⣮| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ��������� |
| T | ʧȥһ�����Ӻ��γ���Ne��ͬ�ĺ�������Ų� |
| X | �����������Ǵ�����������2�� |
| Y | ��ij�ֵ����ǿ�������Ҫ�ɷ֣�Ҳ���������ȼ�� |
| Z | ԭ�Ӻ�����3�����Ӳ㣬�����ȴ������1������ |
��2��Y�γɵ���һ�ֵ��ʣ���Ҫ�����ڵ����ƽ�����У���������������ı���ɡ���õ��ʵĻ�ѧʽ��O3��
��3��Ԫ��Z�ں�ˮ�к����dz��ߣ���ˮ�к�ZԪ�صĻ�������Ҫ��NaCl��д��ѧʽ����
��4������T��ԭ�ӽṹʾ��ͼ��
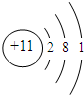 ��
����5����XԪ����ɵĵ�����YԪ����ɵij���������ȼ�գ����ɵIJ�����CO2��CO��
���� ��Tʧȥһ�����Ӻ��γ���Ne��ͬ�ĺ�������Ų�����֪T��������Ϊ11����TΪNaԪ�أ�
X�������������Ǵ�����������2������֪��2�����Ӳ㣬����������Ϊ4��XΪCԪ�أ�
Y�ĵ����ǿ�������Ҫ�ɷ֣�Ҳ���������ȼ������YΪOԪ�أ�
Z��ԭ�Ӻ�����3�����Ӳ㣬�����ȴ������1�����ӣ���֪����������Ϊ7����ZΪClԪ�أ��Դ������
��� �⣺��Tʧȥһ�����Ӻ��γ���Ne��ͬ�ĺ�������Ų�����֪T��������Ϊ11����TΪNaԪ�أ�
X�������������Ǵ�����������2������֪��2�����Ӳ㣬����������Ϊ4��XΪCԪ�أ�
Y�ĵ����ǿ�������Ҫ�ɷ֣�Ҳ���������ȼ������YΪOԪ�أ�
Z��ԭ�Ӻ�����3�����Ӳ㣬�����ȴ������1�����ӣ���֪����������Ϊ7����ZΪClԪ�أ�
��1��Ԫ��X��һ��ͬλ���������ԭ�������ı�������ͬλ�ص�ԭ�ӷ�����612C��X����һ��ͬλ�ؿ������ⶨ�����������������ͬλ�صķ�����614C��
�ʴ�Ϊ��612C��614C��
��2��Y�γɵ���һ�ֵ��ʣ���Ҫ�����ڵ����ƽ�����У���������������ı���ɡ���õ��ʵĻ�ѧʽ��O3���ʴ�Ϊ��O3��
��3��Ԫ��Z�ں�ˮ�к����dz��ߣ���ˮ�к�ZԪ�صĻ�������Ҫ��NaCl���ʴ�Ϊ��NaCl��
��4��TΪNa����ԭ�ӽṹʾ��ͼΪͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5����XԪ����ɵĵ�����YԪ����ɵij���������ȼ�գ����ɵIJ�����CO2��CO���ʴ�Ϊ��CO2��CO��
���� ���⿼��λ�á��ṹ�����ʣ�Ϊ��Ƶ���㣬����ԭ�ӽṹ��Ԫ�ػ�����֪ʶ�ƶ�Ԫ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���

 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�| A�� | ����ͨ��ˮ���ܵ�NH3•H2O | B�� | ʵ�����ô���ʯ��������ȡCO2 | ||
| C�� | ���õ��������� | D�� | ������ˮ����Ϊ����ˮ |
��֪��
��2C3H8��g��+7O2��g��=6CO��g��+8H2O��l������H=-2741.8kJ/mol
��2CO��g��+O2��g��=2CO2��g����H=-566kJ/mol
��1����ӦC3H8��g��+5O2��g��=3CO2��g��+4H2O��l���ġ�H=-2219.9kJ/mol��
��2�����ݣ�1���еķ�Ӧ�������һ������ȼ�ϵ�أ�һ��ͨ���������һ��ͨ��������壻ȼ�ϵ���ڲ������ڵIJ����������ƣ�Y2O3��������ﯣ�ZrO2�����壬�����ڲ����Դ���O2-���ڵ���ڲ�O2-�ƶ�������ڵ�ظ�����Ӧ�����ʷֱ���B
A��������O2 B��������C3H8C��������C3H8 D��������O2
��3��C3H8�ڲ�������������ȼ�գ�����CO��CO2�Լ���̬ˮ�������еIJ���ͨ��һ���̶�������ܱ������У���һ�������·������¿��淴Ӧ��CO ��g��+H2O��g��?CO2��g��+H2 ��g��
��������ʵ��˵���÷�Ӧ�ﵽƽ�����bd��
a����ϵ�е�ѹǿ�������仯 b��������H2��=������CO��
c����������ƽ����Է��������������仯 d��CO2��Ũ�Ȳ��ٷ����仯
��T��ʱ����1L�������У�ͨ��һ������CO��g����H2O��g����������Ӧ�������¶Ȳ��䣬������Ũ����ʱ��仯�����
| ʱ��/min | c��CO�� | c��H2O����g�� | c��CO2�� | c��H2�� |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
����֪420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9�������Ӧ��ʼʱCO��H2O��g����Ũ�ȶ���0.01mol/L����CO�ڴ������µ�ת����Ϊ75%����֪397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12�����жϸ÷�Ӧ�ġ�H��0 �����������=��������������
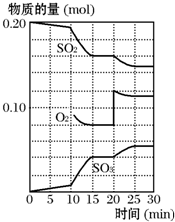 ��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0�� ��
��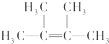 ��������2��3-����-2-��ϩ��
��������2��3-����-2-��ϩ��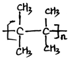 ��
�� ����CH3CH2��2C=CH2������˳���칹����
����CH3CH2��2C=CH2������˳���칹����