题目内容
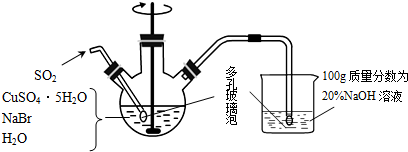
5.一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子.(1)加入铝粉产生H2,说明铝具有还原性(填“氧化性”或“还原性”).
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在.
设计实验证实如下:
| 装置 | 现象 |
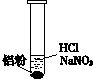 | ⅰ.实验初始,未见明显现象 ⅱ.过一会儿,出现气泡,液面上方呈浅棕色 ⅲ.试管变热,溶液沸腾 |
②根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI-淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI-淀粉试纸检验浅棕色气体 | 试纸变蓝 |
b.实验1的目的是对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能.
c.实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
1Al+1NO3-+4H+═1Al3++1NO↑+2H2O.
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在.
重新设计实验证实如下:
| 装置 | 现象 |
 | ⅰ.实验初始,未见明显现象 ⅱ.过一会儿,出现气泡,有刺激性气味 |
①刺激性气味的气体是NH3.
②产生该气体的离子方程式是8Al+3NO3-+5OH-+2H2O=3NH3↑+8AlO2-.
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(5)实验结果证实:NO3?在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物.习题中的无色溶液一定能大量存在的是Na+和OH-.
分析 无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,因硝酸具有强氧化性,则无色溶液应为NaOH溶液,
(1)加入铝粉产生H2,Al失去电子,H得到电子;
(2)①盐酸与氧化铝反应生成氯化铝和水;
②液面上方呈浅棕色,一定不是氢气,为氮的氧化物,由将湿润KI-淀粉试纸置于空气中未变蓝,说明KI在空气中不能被氧化,而用湿润KI-淀粉试纸检验浅棕色气体试纸变蓝,则KI被氧化,即二氧化氮与水反应生成硝酸,再氧化碘离子生成碘单质;Al与H+、NO3-发生氧化还原反应生成硝酸铝、NO和水;
(3)用湿润KI-淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝,则气体为氨气,碱性条件下Al与NO3-发生氧化还原反应生成氨气;
(4)NaOH溶液中加入铝粉,结果只检验出有H2生成,即反应生成偏铝酸钠和氢气.
解答 解:无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,因硝酸具有强氧化性,则无色溶液应为NaOH溶液,
(1)加入铝粉产生H2,Al失去电子,H得到电子,则Al为还原剂,具有还原性,故答案为:还原性;
(2)①盐酸与氧化铝反应生成氯化铝和水,该离子反应为6H++Al2O3═2Al3++3H2O,故答案为:6H++Al2O3═2Al3++3H2O;
②液面上方呈浅棕色,一定不是氢气,为氮的氧化物,由将湿润KI-淀粉试纸置于空气中未变蓝,说明KI在空气中不能被氧化,而用湿润KI-淀粉试纸检验浅棕色气体试纸变蓝,则KI被氧化,即二氧化氮与水反应生成硝酸,再氧化碘离子生成碘单质,
a.由上述分析可知,浅棕色气体是NO2,故答案为:NO2;
b.实验1的目的是对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能,故答案为:对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能;
c.Al与H+、NO3-发生氧化还原反应生成硝酸铝、NO和水,离子反应为Al+NO3?+4H+═Al3++NO↑+2H2O,故答案为:1;1;4;H+;1;1;2;H2O;
(3)①用湿润KI-淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝,则气体为NH3,故答案为:NH3;
②由上述分析可知,碱性条件下Al与NO3-发生氧化还原反应生成氨气,离子反应为8Al+3NO3-+5OH-+2H2O═3NH3↑+8AlO2-,
故答案为:8Al+3NO3-+5OH-+2H2O═3NH3↑+8AlO2-;
(4)NaOH溶液中加入铝粉,结果只检验出有H2生成,即反应生成偏铝酸钠和氢气,反应为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
点评 本题考查物质中的成分及性质,为高频考点,把握实验方案的设计及发生的氧化还原反应为解答的关键,注意设计思路与物质性质的关系,侧重实验学生分析能力、综合应用能力的考查,较好考查学生实验基本技能,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 加催化剂 | B. | 升高温度 | C. | 减小压强 | D. | 加入O2 |
| A. | 在一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 | |
| B. | 当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 | |
| C. | 单位时间内生成CO和Cl2的物质的量比为1:1时,反应达到平衡状态 | |
| D. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| A. | C的体积分数降低 | B. | x+y>z | ||
| C. | 平衡向正反应方向移动 | D. | x+y<z |
| A. | 保持体积不变加入H2 | B. | 压缩体积至原来的一半 | ||
| C. | 降低温度 | D. | 加入催化剂 |
| A. |  和 和 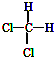 是两种种不同的物质 是两种种不同的物质 | |
| B. | 由乙烯之间的相互加成可以得到聚乙烯 | |
| C. | 丁烷与丁烯互为同系物 | |
| D. | 乙酸不能使紫色石蕊变红 |
| A. | F | B. | N | C. | O | D. | H |