题目内容
8.运用元素周期律分析下面的推断,其中不正确的是( )| A. | 铍的氧化物对应的水化物具有两性 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,钠的燃烧产物比铷(Rb)的燃烧产物更复杂 | |
| D. | 硫酸锶(SrSO4)是难溶于水的白色固体 |
分析 A.Be与Al位于对角线,氧化物性质相似;
B.卤素单质从上到下单质的颜色加深,状态由气体、液体、固体变化,AgX不溶于水和硝酸,只有AgF溶于水;
C.金属性越强,与氧气反应的产物越复杂;
D.硫酸钡不溶于水,同族化合物性质相似.
解答 解:A.Be与Al位于对角线,可知铍的氧化物对应的水化物具有两性,故A正确;
B.卤素单质从上到下单质的颜色加深,状态由气体、液体、固体变化,AgX不溶于水和硝酸,只有AgF溶于水,则砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸,故B正确;
C.金属性Rb大于Na,在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂,故C错误;
D.硫酸钡不溶于水,同族化合物性质相似,则硫酸锶(SrSO4)是难溶于水的白色固体,故D正确;
故选C.
点评 本题考查周期表与周期律的应用,为高频考点,把握元素的位置、元素周期律、元素化合物知识为解答该题的关键,侧重于学生的分析能力和应用能力的考查,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
20.海水中蕴藏着丰富的资源,海水综合利用的流程图如图1:
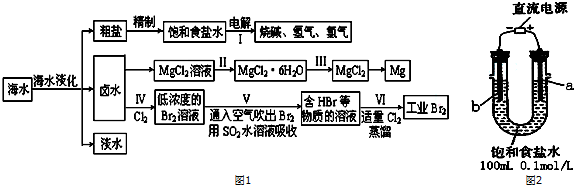
(一)某化学研究小组用图2装置模拟步骤I电解食盐水(用铁和石墨做电极).
(1)a电极材料是石墨(填铁、石墨),其电极反应式为2Cl--2e-=Cl2↑.
(2)当阴极产生11.2mL气体时(标准状况),该溶液的pH为12(忽略反应前后溶液体积的变化).
(二)卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+.下表是生成氢氧化物沉淀的pH:
(3)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,可选用的物质是b(填序号,下同),加入c调节溶液的pH,充分反应后过滤,可得MgCl2溶液.
a.KMnO4 b.H2O2 c.MgO d.NaOH
(4)步骤Ⅲ由MgCl2•H2O获得MgCl2的操作是:将MgCl2•6H2O在干燥的HCl气流中加热.
(三)制取工业溴:
(5)步骤Ⅳ中已获得Br2,步骤Ⅴ中又将Br2还原为Br-,其目的是富集溴元素.
(6)写出步骤Ⅴ用SO2水溶液吸收Br2的离子方程式:Br2+SO2+2H2O=4H++SO42-+2Br-.

(一)某化学研究小组用图2装置模拟步骤I电解食盐水(用铁和石墨做电极).
(1)a电极材料是石墨(填铁、石墨),其电极反应式为2Cl--2e-=Cl2↑.
(2)当阴极产生11.2mL气体时(标准状况),该溶液的pH为12(忽略反应前后溶液体积的变化).
(二)卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+.下表是生成氢氧化物沉淀的pH:
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
| 完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
a.KMnO4 b.H2O2 c.MgO d.NaOH
(4)步骤Ⅲ由MgCl2•H2O获得MgCl2的操作是:将MgCl2•6H2O在干燥的HCl气流中加热.
(三)制取工业溴:
(5)步骤Ⅳ中已获得Br2,步骤Ⅴ中又将Br2还原为Br-,其目的是富集溴元素.
(6)写出步骤Ⅴ用SO2水溶液吸收Br2的离子方程式:Br2+SO2+2H2O=4H++SO42-+2Br-.
19.人们研究发现金星大气中有一种称之为硫化羰(COS)的分子,其结构与CO2类似,硫化羰是一种与生命密切相关的物质,下列有关COS的推测肯定不正确的是( )
| A. | COS分子是含有极性键的极性分子 | |
| B. | COS属于离子化合物 | |
| C. | COS的结构式为S=C=O | |
| D. | COS分子中所有原子都满足8电子稳定结构 |
16.下列说法正确的是( )
| A. | 苯酚有毒,不可以作消毒剂和防腐剂 | |
| B. | 橙色的K2Cr2O7酸性水溶液遇到乙醇迅速生成蓝绿色Cr3+是由于乙醇有还原性 | |
| C. | 所有卤代烃均可以发生消去反应和水解反应 | |
| D. | 用食醋去除水壶中的水垢时所发生的是水解反应 |
3.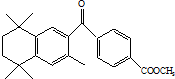 蓓萨罗丁是一种治疗顽固性皮肤T-细胞淋巴瘤的药物,其结构简式如图,下列关于蓓萨罗丁判断正确的是( )
蓓萨罗丁是一种治疗顽固性皮肤T-细胞淋巴瘤的药物,其结构简式如图,下列关于蓓萨罗丁判断正确的是( )
 蓓萨罗丁是一种治疗顽固性皮肤T-细胞淋巴瘤的药物,其结构简式如图,下列关于蓓萨罗丁判断正确的是( )
蓓萨罗丁是一种治疗顽固性皮肤T-细胞淋巴瘤的药物,其结构简式如图,下列关于蓓萨罗丁判断正确的是( )| A. | 蓓萨罗丁的分子式为C24H28O3 | |
| B. | 蓓萨罗丁分子中一定有17个碳原子在同一平面内 | |
| C. | 蓓萨罗丁可以与氢气发生加成反应,1mol蓓萨罗丁最多消耗8 mol H2 | |
| D. | 蓓萨罗丁能与NaOH溶液反应,但是不能使酸性KMnO4溶液褪色 |
13.下列化学用语正确的是( )
| A. | N2的电子式: | B. | H2O2的电子式 | ||
| C. | 氨分子的结构式 | D. | 14C的原子结构示意图 |
20.下列叙述错误的是( )
| A. | 在所有元素中氢原子半径最小 | |
| B. | Al3+、Na+、O2-微粒半径依次增大 | |
| C. | P、S、Cl最高正价依次升高 | |
| D. | 锂、钠、钾、铷、铯单质的熔点逐渐升高 |
17.设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 常温常压下,32gO2和O3的混合气体所含质子数一定为16NA | |
| B. | 标准状况下,11.2LSO2中含有的分子数为0.5NA | |
| C. | 常温下,5.6 g铁与硝酸反应,失去的电子数一定为0.3 NA | |
| D. | 23g钠与足量氧气充分反应,转移的电子数一定是NA |
18.以下工业生产过程不涉及化学变化是( )
| A. | 煤的液化 | B. | 石油分馏 | C. | 煤的干馏 | D. | 重油催化裂化 |