题目内容
19.人们研究发现金星大气中有一种称之为硫化羰(COS)的分子,其结构与CO2类似,硫化羰是一种与生命密切相关的物质,下列有关COS的推测肯定不正确的是( )| A. | COS分子是含有极性键的极性分子 | |
| B. | COS属于离子化合物 | |
| C. | COS的结构式为S=C=O | |
| D. | COS分子中所有原子都满足8电子稳定结构 |
分析 硫化羰(COS)的分子,其结构与CO2类似,结构为S=C=O,为直线结构,只含共价键,所有原子满足最外层8电子稳定结构,以此来解答.
解答 解:A.结构为S=C=O,为直线结构,含极性键,但正负电荷中心不重合,为极性分子,故A正确;
B.只含共价键,为共价化合物,故B错误;
C.与CO2类似,结构为S=C=O,故C正确;
D.结构为S=C=O,S、O最外层电子数为6,则分子中所有原子都满足8电子稳定结构,故D正确;
故选B.
点评 本题考查化学键及分子结构,为高频考点,把握信息及结构相似为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.

练习册系列答案
相关题目
11.NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 标准状况下,11.2L的乙烷所含的分子数为0.5NA | |
| B. | 0.5mol C3H8分子中含C-H共价键4NA | |
| C. | 11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
7.部分中学化学常见元素的原子结构和性质如下表所示:
请用元素符号或化学式回答下列问题:
(1)C、D、E的简单离子的半径由大到小的顺序为N3->Na+>Al3+.
(2)B元素有多种同位素,写出其中带8个中子的原子符号146C.
(3)由A和C组成的六原子化合物甲(C2A4)可用作发射卫星时的燃料,用NO2为氧化剂,这两种物质反应生成氮气和水蒸气.已知:
①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1
②甲(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1
写出甲与NO2反应的热化学方程式2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ•mol-1.
(4)A与C能形成离子化合物A5C,A5C中既含离子键又含共价键,其电子式为 ,该物质能与水剧烈反应生成两种气体,写出其反应的化学方程式NH4H=NH3↑+H2↑.
,该物质能与水剧烈反应生成两种气体,写出其反应的化学方程式NH4H=NH3↑+H2↑.
(5)E的单质可以和D的最高价氧化物对应的水化物反应,写出其反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,F的最高价氧化物对应的水化物和E的最高价氧化物对应的水化物可以发生反应,试写出其反应的离子方程式3H++Al(OH)3=Al3++3H2O.
| 元素代号 | 部分特征 |
| A | 气态单质在标准状况下密度是0.0893g/L |
| B | 形成的化合物的种类最多 |
| C | 形成的氧化物的种类最多 |
| D | 形成的化合物焰色反应呈黄色 |
| E | 生活中常用的金属,在空气中表面通常形成一层致密的氧化膜 |
| F | 最高价氧化物对应的水化物酸性在短周期中最强 |
(1)C、D、E的简单离子的半径由大到小的顺序为N3->Na+>Al3+.
(2)B元素有多种同位素,写出其中带8个中子的原子符号146C.
(3)由A和C组成的六原子化合物甲(C2A4)可用作发射卫星时的燃料,用NO2为氧化剂,这两种物质反应生成氮气和水蒸气.已知:
①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1
②甲(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1
写出甲与NO2反应的热化学方程式2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ•mol-1.
(4)A与C能形成离子化合物A5C,A5C中既含离子键又含共价键,其电子式为
 ,该物质能与水剧烈反应生成两种气体,写出其反应的化学方程式NH4H=NH3↑+H2↑.
,该物质能与水剧烈反应生成两种气体,写出其反应的化学方程式NH4H=NH3↑+H2↑.(5)E的单质可以和D的最高价氧化物对应的水化物反应,写出其反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,F的最高价氧化物对应的水化物和E的最高价氧化物对应的水化物可以发生反应,试写出其反应的离子方程式3H++Al(OH)3=Al3++3H2O.
4.A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由大到小的顺序是( )
| A. | A、B、C、D、E | B. | E、C、D、A、B | C. | B、A、D、C、E | D. | C、D、E、B、A |
11.下列化学用语表述正确的是( )
| A. | 羟基的电子式: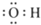 | B. | 醛基的结构简式-COH | ||
| C. | 乙烯分子的最简式:CH2 | D. | 1,2-二溴乙烷的结构简式:C2H4Br2 |
8.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 铍的氧化物对应的水化物具有两性 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,钠的燃烧产物比铷(Rb)的燃烧产物更复杂 | |
| D. | 硫酸锶(SrSO4)是难溶于水的白色固体 |
 .
.