题目内容
3.下列变化需加入氧化剂才可实现的是( )| A. | CO→CO2 | B. | CO2→Na2CO3 | C. | NO2→HNO3 | D. | S→CuS |
分析 需加入氧化剂才能实现,说明题中物质应具有还原性,被氧化,所含元素的化合价应升高,以此解答该题.
解答 解:A.C元素化合价升高,被氧化,应加入氧化剂才能实现,故A正确;
B.元素化合价不变,不是氧化还原反应,故B错误;
C.无需加入氧化剂,二氧化氮和水反应可生成硝酸,故C错误;
D.S元素化合价降低,被还原,应加入还原剂,故D错误.
故选A.
点评 本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力的考查,明确元素化合价的变化为解答该题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.苹果汁是人们喜爱的饮料,由于含有Fe2+,现榨的苹果汁会由淡绿色变为棕黄色,在这种苹果汁中加入维生素C,可避免该现象,这些现象体现了( )
| A. | Fe2+具有氧化性,维生素C具有还原性 | |
| B. | Fe2+具有氧化性,维生素C也具有氧化性 | |
| C. | Fe2+具有还原性,维生素C具有氧化性 | |
| D. | Fe2+具有还原性,维生素C也具有还原性 |
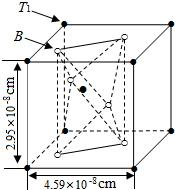
11.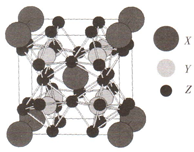 某种能实现热电效应的晶体的晶胞模型如右图.已知晶胞的六个面的原子数相同,Y原子位于Z原子围成的八面体中心.下列说法正确的是( )
某种能实现热电效应的晶体的晶胞模型如右图.已知晶胞的六个面的原子数相同,Y原子位于Z原子围成的八面体中心.下列说法正确的是( )
 某种能实现热电效应的晶体的晶胞模型如右图.已知晶胞的六个面的原子数相同,Y原子位于Z原子围成的八面体中心.下列说法正确的是( )
某种能实现热电效应的晶体的晶胞模型如右图.已知晶胞的六个面的原子数相同,Y原子位于Z原子围成的八面体中心.下列说法正确的是( )| A. | 距离X最近的Y原子有8个 | B. | 距离X最近的X原子有6个 | ||
| C. | 距离X最近的Z原子有3个 | D. | 该晶体的化学式为X2Y8Z12 |
18.实验室里需储存在棕色试剂瓶中的是( )
| A. | 金属钠 | B. | 浓硝酸 | C. | FeSO4溶液 | D. | 浓硫酸 |
15.常温下,下列各溶液中,可能大量共存的离子组是( )
| A. | pH=0的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | c(H+)=1×10-14mol•L-1的溶液中:Mg2+、NO3-、Fe2+、ClO- | |
| C. | 含有大量Fe3+的溶液中:Na+、I-、K+、NO3- | |
| D. | 由水电离出的c(OH-)=1×10-13mol/L的溶液中:Na+、[Al(OH)4]-、S2-、CO32- |
12.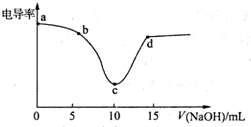 利用电导率传感器可绘制电导率曲线图,下图为用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1盐酸过程中的电导率曲线.下列说法错误的是( )
利用电导率传感器可绘制电导率曲线图,下图为用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1盐酸过程中的电导率曲线.下列说法错误的是( )
 利用电导率传感器可绘制电导率曲线图,下图为用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1盐酸过程中的电导率曲线.下列说法错误的是( )
利用电导率传感器可绘制电导率曲线图,下图为用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1盐酸过程中的电导率曲线.下列说法错误的是( )| A. | 电导率传感器能用于判断酸碱中和滴定的终点 | |
| B. | 该过程中,a点所示溶液的导电性最强 | |
| C. | c点电导率最小是因为此时溶液中导电微粒的数目最少 | |
| D. | d点所示溶液中存在:c(Cl-)+c(OH-)=c(H+)+c(Na+) |
12.下列说法错误的是( )
| A. | 浓硝酸与足量铜片反应时,先生成红棕色气体,后生成无色气体 | |
| B. | 浓硫酸具有强氧化性,常温下可将铝的单质氧化,因此,不能用铝罐车运输浓硫酸 | |
| C. | 饱和氯水既有酸性又有漂白性,加入NaHCO₃后漂白性减弱 | |
| D. | 浓盐酸与足量二氧化锰反应后,盐酸有剩余 |