题目内容
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是( )
| 放电 |
| 充电 |
下列叙述不正确的是( )
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、放电时每转移3 mol电子,正极有1mol K2FeO4被还原 |
| C、充电时阳极反应为:Fe(OH)3-3e-+5 OH-=FeO42-+4H2O |
| D、放电时正极附近溶液的碱性减弱 |
考点:化学电源新型电池
专题:电化学专题
分析:根据电池反应式知,放电时,锌失电子而作负极,电极反应式为Zn-2e-+2OH-=Zn(OH)2,高铁酸钾得电子而作正极,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,充电时,充电时,阳极反应和放电时的正极反应是互为逆反应,阴极上的反应和放电时的负极反应是互为逆反应.
解答:
解:A.放电时,Zn失去电子,发生Zn-2e-+2OH-=Zn(OH)2,故A正确;
B.放电时Zn元素失去电子,正极K2FeO4中Fe元素得到电子,转移电子数为1mol×(6-3)=3mol,故B正确;
C.充电时,阳极上铁离子失去电子,发生Fe(OH)3转化为FeO42-的反应,电极反应为Fe(OH)3-3e-+5OH-=FeO42-+4H2O,故C正确;
D.放电时正极反应为:FeO42-+4H2O+3e=Fe(OH)3-+5OH-,生成氢氧根离子,所以正极附近溶液的碱性增强,故D错误;
故选D.
B.放电时Zn元素失去电子,正极K2FeO4中Fe元素得到电子,转移电子数为1mol×(6-3)=3mol,故B正确;
C.充电时,阳极上铁离子失去电子,发生Fe(OH)3转化为FeO42-的反应,电极反应为Fe(OH)3-3e-+5OH-=FeO42-+4H2O,故C正确;
D.放电时正极反应为:FeO42-+4H2O+3e=Fe(OH)3-+5OH-,生成氢氧根离子,所以正极附近溶液的碱性增强,故D错误;
故选D.
点评:本题考查电解池与原电池,明确电极反应中放电为原电池、充电为电解池时解答本题的关键,题目难度不大.

练习册系列答案
相关题目
由CO、CO2组成的混合气体36g,其中含C原子数为NA个,则C、O原子个数比为( )
| A、1:3 | B、2:3 |
| C、1:1 | D、4:3 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、16gO2中含有的氧分子数为NA |
| B、1mol镁原子中含有的电子数为NA |
| C、常温常压下,11.2L H2中含有的氢分子数为0.5NA |
| D、1L 1mol/L BaCl2溶液中含有的钡离子数为NA |
若1mol某烷烃燃烧后,测得产物中含有m mol CO2和n mol CO,则该烷烃分子中氢原子个数为( )
| A、m+n |
| B、2(m+n) |
| C、m-n+2 |
| D、2(n+m+1) |
下列电离方程式不正确的是( )
| A、H2SO4═2H++SO42- |
| B、NH4NO3═NH4++NO3- |
| C、Ba(OH)2═Ba2 ++2OH- |
| D、Na2CO3═Na2++CO32- |
原电池在工作时,发生氧化还原反应,下列反应不可能作为原电池工作时发生的反应的是( )
| A、Cu+2AgNO3═Cu(NO3)2+2Ag |
| B、2Fe+O2+2H2O═2Fe(OH)2 |
| C、NaOH+HCl═NaCl+H2O |
| D、2H2+O2═2H2O |
下列电子式书写正确的是( )
A、 |
B、 |
C、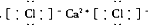 |
D、 |
某恒温密闭容器中,可逆反应A(s)?B(?)+C(g)△H=+QKJ/mol(Q>0),达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A、产物B的状态可能为气态、固态或液态 |
| B、平衡时,单位时间内m(A)消耗﹕m(C)消耗=1﹕1 |
| C、保持体积不变,向平衡体系中加入B,平衡可能不移动 |
| D、若开始时向容器中加入1molB和1molC,达到平衡时放出热量QKJ |