题目内容
原电池在工作时,发生氧化还原反应,下列反应不可能作为原电池工作时发生的反应的是( )
| A、Cu+2AgNO3═Cu(NO3)2+2Ag |
| B、2Fe+O2+2H2O═2Fe(OH)2 |
| C、NaOH+HCl═NaCl+H2O |
| D、2H2+O2═2H2O |
考点:原电池和电解池的工作原理,氧化还原反应
专题:电化学专题
分析:原电池工作时发生的反应是一个氧化还原反应,氧化还原反应的特征是有元素化合价的变化的反应来分析判断.
解答:
解:A、属于氧化还原反应,能作为原电池工作时发生的反应,故A错误;
B、属于氧化还原反应,能作为原电池工作时发生的反应,故B错误;
C、不属于氧化还原反应,不能作为原电池工作时发生的反应,故C正确;
D、属于氧化还原反应,能作为原电池(燃料电池)工作时发生的反应,故D错误;
故选C.
B、属于氧化还原反应,能作为原电池工作时发生的反应,故B错误;
C、不属于氧化还原反应,不能作为原电池工作时发生的反应,故C正确;
D、属于氧化还原反应,能作为原电池(燃料电池)工作时发生的反应,故D错误;
故选C.
点评:本题考查学生电化学中有关氧化还原反应的概念知识,注重基础知识的考查,难度不大.

练习册系列答案
相关题目
下列物质都是食品添加剂,但使用时必须严格控制用量的是( )
| A、食醋 | B、蔗糖 |
| C、料酒 | D、亚硝酸钠 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是( )
| 放电 |
| 充电 |
下列叙述不正确的是( )
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、放电时每转移3 mol电子,正极有1mol K2FeO4被还原 |
| C、充电时阳极反应为:Fe(OH)3-3e-+5 OH-=FeO42-+4H2O |
| D、放电时正极附近溶液的碱性减弱 |
下列化学反应,能用离子方程式CO
+2H+═CO2↑+H2O来表示的是( )
2- 3 |
| A、稀硝酸和碳酸钡的反应 |
| B、稀硝酸和碳酸钾溶液的反应 |
| C、石灰石和盐酸的反应 |
| D、盐酸和NaHCO3溶液的反应 |
确定乙酸是弱酸的依据是( )
| A、乙酸可以和乙醇发生酯化反应 |
| B、乙酸钠的水溶液显碱性 |
| C、乙酸能使石蕊试液变红 |
| D、Na2CO3中加入乙酸产生CO2 |
分子式为C5H12O的醇催化氧化得到的有机物不能发生银镜反应的醇有( )
| A、8种 | B、7种 | C、5种 | D、3种 |
下列电解质的电离方程式书写正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、KClO3═K++Cl-+3O2- |
| C、NaHSO4═Na++H++SO42- |
| D、NH3?H2O═NH4++OH- |
对于有机物 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、该物质的分子式为C10H12 |
| B、该物质能与4mol Br2完全加成 |
| C、该物质能发生加聚反应 |
| D、该物质苯环上的一氯代物有3种 |
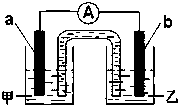 一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-=2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-=2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题: