题目内容
实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.如图1是煤化工产业链的一部分,试运用所学知识,解决下列问题:

(1)该产业链中属于高中阶段常见的在低温下能自发进行的反应是:
(2)已知该产业链中某反应的平衡表达式为K=
:它所对应的化学反应为:
(3)已知在一定温度下,
C(s)+CO2(g)?2CO(g)平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数K2;
C(s)+H2O(g)?CO(g)+H2(g) 平衡常数K3;
则K1、K2、K3之间的关系是: .
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
该反应的正反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为: .
(5)从图1看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.对反应N2O4(g)?2NO2(g)△H>0在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是 .
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点的化学平衡常数:A>C
(6)0.2mol/L的NaOH与0.4mol/L的上述产业链中一产品化肥硝酸铵溶液等体积混合后,溶液中各离子的物质的量浓度从大到小的顺序是 .

(1)该产业链中属于高中阶段常见的在低温下能自发进行的反应是:
(2)已知该产业链中某反应的平衡表达式为K=
| c(H2)c(CO) |
| c(H2O) |
(3)已知在一定温度下,
C(s)+CO2(g)?2CO(g)平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数K2;
C(s)+H2O(g)?CO(g)+H2(g) 平衡常数K3;
则K1、K2、K3之间的关系是:
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(5)从图1看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.对反应N2O4(g)?2NO2(g)△H>0在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点的化学平衡常数:A>C
(6)0.2mol/L的NaOH与0.4mol/L的上述产业链中一产品化肥硝酸铵溶液等体积混合后,溶液中各离子的物质的量浓度从大到小的顺序是
考点:化学平衡的计算,用化学平衡常数进行计算,化学平衡的影响因素
专题:化学平衡专题
分析:(1)生产氨气的反应放出大量的热,△G<0能自发进行;
(2)根据平衡常数的定义判断反应的方程式;
(3)根据平衡常数的表达式推断;
(4)根据温度变化平衡常数的变化判断温度对化学平衡移动的影响,进而判断反应热,利用三段式法计算转化率;
(5)根据从平衡移动的角度分析各物理量的变化;
(6)考虑氨水为弱电解质,从弱电解质的电离和盐类的水解两个角度比较离子浓度的大小.
(2)根据平衡常数的定义判断反应的方程式;
(3)根据平衡常数的表达式推断;
(4)根据温度变化平衡常数的变化判断温度对化学平衡移动的影响,进而判断反应热,利用三段式法计算转化率;
(5)根据从平衡移动的角度分析各物理量的变化;
(6)考虑氨水为弱电解质,从弱电解质的电离和盐类的水解两个角度比较离子浓度的大小.
解答:
解:(1)生产氨气的反应放出大量的热,△G<0能自发进行,氨水呈碱性,与酸发生中和反应,属于放热反应,在低温下易进行,故答案为:N2+3H2 2NH3或NH3+HNO3═NH4NO3;
2NH3或NH3+HNO3═NH4NO3;
(2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,所以该反应的方程式为:C(s)+H2O(g) CO(g)+H2(g),故答案为:C(s)+H2O(g)
CO(g)+H2(g),故答案为:C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
(3)根据化学方程式可知:K1=
,K2=
,K3=
,所以:K3=
×
=
=K1×K2,
故答案为:K3=K1×K2;
(4)由表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,说明正反应为让热反应,
设平衡时转化的CO为xmol/L,
利用三段式法计算:
CO(g)+H2O(g)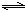 H2(g)+CO2(g),
H2(g)+CO2(g),
起始:0.020mol/L 0.020mol/L 0 0
转化:xmol/L xmol/L x mol/L x mol/L
平衡:(0.02-x)mol/L:(0.02-x)mol/L xmol/L xmol/L
则有:
=9
解之得:x=0.015,
所以转化率为:
=75%,故答案为:放热;75%;
(5)在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确,
E.A、C两点温度相同,化学平衡常数应相等,故E错误;
故选:D;
(6)0.2mol/L的NaOH与0.4mol/L的上述产业链中一产品化肥硝酸铵溶液等体积混合后,设溶液的体积为1L,则反应后溶液中含有n(NO3-)=0.4mol,n(Na+)=0.2mol,
n(NH4+)=0.2mol,n(NH3?H2O)=0.2mol,反应溶液呈碱性,NH3?H2O继续电离出NH4+离子,则c(NH4+)>c(Na+)>c(NH3?H2O),由于弱电解质的电离程度较小,
则c(NH3?H2O)>c(OH-),溶液呈碱性,则c(OH-)>c(H+),
所以各离子的物质的量浓度从大到小的顺序是c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),
故答案为:c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+).
 2NH3或NH3+HNO3═NH4NO3;
2NH3或NH3+HNO3═NH4NO3;(2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,所以该反应的方程式为:C(s)+H2O(g)
 CO(g)+H2(g),故答案为:C(s)+H2O(g)
CO(g)+H2(g),故答案为:C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);(3)根据化学方程式可知:K1=
| c 2(CO) |
| c(CO 2) |
| c(H 2)×c(CO 2) |
| c(CO)×c(H 2O) |
| c(CO)×c(H2) |
| c(H 2O) |
| c(H 2)×c(CO 2) |
| c(CO)×c(H 2O) |
| c 2(CO) |
| c(CO 2) |
| c(CO)×c(H2) |
| c(H 2O) |
故答案为:K3=K1×K2;
(4)由表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,说明正反应为让热反应,
设平衡时转化的CO为xmol/L,
利用三段式法计算:
CO(g)+H2O(g)
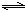 H2(g)+CO2(g),
H2(g)+CO2(g),起始:0.020mol/L 0.020mol/L 0 0
转化:xmol/L xmol/L x mol/L x mol/L
平衡:(0.02-x)mol/L:(0.02-x)mol/L xmol/L xmol/L
则有:
| x?x |
| (0.020-x)?(0.020-x) |
解之得:x=0.015,
所以转化率为:
| 0.015 |
| 0.02 |
(5)在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确,
E.A、C两点温度相同,化学平衡常数应相等,故E错误;
故选:D;
(6)0.2mol/L的NaOH与0.4mol/L的上述产业链中一产品化肥硝酸铵溶液等体积混合后,设溶液的体积为1L,则反应后溶液中含有n(NO3-)=0.4mol,n(Na+)=0.2mol,
n(NH4+)=0.2mol,n(NH3?H2O)=0.2mol,反应溶液呈碱性,NH3?H2O继续电离出NH4+离子,则c(NH4+)>c(Na+)>c(NH3?H2O),由于弱电解质的电离程度较小,
则c(NH3?H2O)>c(OH-),溶液呈碱性,则c(OH-)>c(H+),
所以各离子的物质的量浓度从大到小的顺序是c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),
故答案为:c(NO3-)>c(NH4+)>c(Na+)>c(OH-)>c(H+).
点评:本题考查较为综合,涉及知识点较多,难度较大,易错点为(1)和(6),注意把握比较溶液离子浓度的方法.

练习册系列答案
相关题目
香叶醇是合成玫瑰香油的主要原料,其结构简式如下:下列有关香叶醇的叙述正确的是( )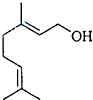

| A、香叶醇的分子式为C10H20O |
| B、不能使溴的四氯化碳溶液褪色 |
| C、不能发生催化氧化反应生成醛 |
| D、既能发生加成反应又能发生取代反应 |
已知25℃时合成氨反应的热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol.一定压强下,向10L的密闭容器里充入1mol N2和3mol H2,达到平衡后,NH3的体积分数为60%.若相同条件下,向同一密闭容器里改充入2mol NH3,产生的热效应为a,此时NH3的转化率为α.则下列判断正确的是( )
| A、a=-23.1kJα=40% |
| B、a=-23.1kJ α=25% |
| C、a=+23.1kJα=40% |
| D、a=+23.1kJ α=25% |
32g某一元醇跟足量的金属钠完全反应,可以得到11.2L(标准状况)氢气,该醇是( )
| A、CH3OH |
| B、C2H5OH |
| C、C3H7OH |
| D、C4H9OH |
热水瓶胆镀银常用的还原剂是( )
| A、福尔马林 | B、银氨溶液 |
| C、葡萄糖 | D、蔗糖 |

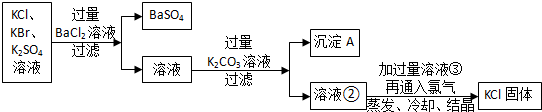
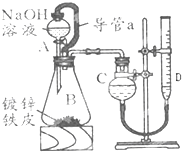 “白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案.
“白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案.