题目内容
文献资料显示某地区的酸雨主要为硫酸型和盐酸型酸雨.某兴趣小组对酸雨进行实验研究.
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HCl外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有 .
(2)设计实验方案验证以上假设.在答题卡上写出实验步骤、预期现象和结论.限选试剂及仪器:盐酸、硝酸、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管.
(3)酸雨部分组成测定:
①标准溶液配制:实验室用1.000mol?L-1较浓的碘水配制250mL 0.02000mol?L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需 .
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴 溶液作指示剂,将0.02000mol?L-1碘水
装入50mL酸式滴定管,滴定终点现象为 ,记录数据,重复滴定2次,平均消耗碘水VmL.
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HCl外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有
(2)设计实验方案验证以上假设.在答题卡上写出实验步骤、预期现象和结论.限选试剂及仪器:盐酸、硝酸、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量酸雨于A、B两支洁净试管中,待用 | 无明显现象 |
| 步骤2:往A试管中加入过量的Ba(OH)2溶液,静置,过滤 | 有白色沉淀 |
| 步骤3:取少量步骤2得到的滤渣加入过量盐酸 | 滤渣不能完全溶解,说明酸雨中含有硫酸 |
| 步骤4:取适量步骤2得到的滤液, | |
| 步骤5:往B试管中加入 振荡 |
①标准溶液配制:实验室用1.000mol?L-1较浓的碘水配制250mL 0.02000mol?L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴
装入50mL酸式滴定管,滴定终点现象为
考点:性质实验方案的设计
专题:实验设计题
分析:(1)依据硫酸型酸雨的形成过程分析,硫酸型酸雨是二氧化硫氧化为三氧化硫溶于水生成硫酸,或二氧化硫和水反应生成亚硫酸,亚硫酸钡氧化为硫酸;
(2)依据实验步骤分析,A试管中加入氢氧化钡溶液后,硫酸根离子全部沉淀后,取滤液加入硝酸酸化的硝酸银检验是否含有盐酸;
B试管中加入品红若出现红色褪去证明酸雨中含有亚硫酸或二氧化硫;
(3)①依据溶液配制的步骤和方法分析需要的玻璃仪器;
②标准液是碘水溶液,滴定和亚硫酸或二氧化碳反应生成硫酸和碘化氢,用淀粉溶液指示反应终点,依据滴入最后一滴碘水溶液呈蓝色且半分钟不褪色证明反应达到终点;
(2)依据实验步骤分析,A试管中加入氢氧化钡溶液后,硫酸根离子全部沉淀后,取滤液加入硝酸酸化的硝酸银检验是否含有盐酸;
B试管中加入品红若出现红色褪去证明酸雨中含有亚硫酸或二氧化硫;
(3)①依据溶液配制的步骤和方法分析需要的玻璃仪器;
②标准液是碘水溶液,滴定和亚硫酸或二氧化碳反应生成硫酸和碘化氢,用淀粉溶液指示反应终点,依据滴入最后一滴碘水溶液呈蓝色且半分钟不褪色证明反应达到终点;
解答:
解:(1)酸雨主要为硫酸型和盐酸型酸雨,硫酸型酸雨是二氧化硫氧化为三氧化硫溶于水生成硫酸,或二氧化硫和水反应生成亚硫酸,亚硫酸钡氧化为硫酸,该酸雨中的溶质除H2SO4、HC1外,根据硫酸型酸雨的形成过程,预测主要溶质还一定有SO2 或H2SO3,
故答案为:SO2 或H2SO3;
(2)实验步骤分析,步骤4中,A试管中加入氢氧化钡溶液后,硫酸根离子全部沉淀后,取滤液加入硝酸酸化的硝酸银检验是否含有盐酸;
步骤5中,B试管中加入品红若出现红色褪去证明酸雨中含有亚硫酸或二氧化硫,
故答案为:
(3)①依据溶液配制步骤分析可知,配制溶液所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需250 mL 容量瓶、胶头滴管,
故答案为:250 mL 容量瓶、胶头滴管;
②标准液是碘水溶液,滴定和亚硫酸或二氧化碳反应生成硫酸和碘化氢,用淀粉溶液指示反应终点,依据滴入最后一滴碘水溶液呈蓝色且半分钟不褪色证明反应达到终点;故答案为:淀粉;滴入一滴碘水溶液由无色变为蓝色,且半分钟不褪色;
故答案为:SO2 或H2SO3;
(2)实验步骤分析,步骤4中,A试管中加入氢氧化钡溶液后,硫酸根离子全部沉淀后,取滤液加入硝酸酸化的硝酸银检验是否含有盐酸;
步骤5中,B试管中加入品红若出现红色褪去证明酸雨中含有亚硫酸或二氧化硫,
故答案为:
| 步骤4:取适量步骤2得到的滤液, 先加入过量稀硝酸,然后加入硝酸银溶液 | 若产生白色沉淀,则酸雨中含有盐酸 |
| 步骤5:往B试管中加入少量品红溶液,振荡 | 若品红溶液褪色,则酸雨含有亚硫酸或二氧化硫 |
故答案为:250 mL 容量瓶、胶头滴管;
②标准液是碘水溶液,滴定和亚硫酸或二氧化碳反应生成硫酸和碘化氢,用淀粉溶液指示反应终点,依据滴入最后一滴碘水溶液呈蓝色且半分钟不褪色证明反应达到终点;故答案为:淀粉;滴入一滴碘水溶液由无色变为蓝色,且半分钟不褪色;
点评:本题考查了二氧化硫性质分析,酸雨成分的实验设计和现象判断,溶液配制步骤和滴定实验的过程应用和计算,题目难度中等.

练习册系列答案
相关题目
下列离子或分子在溶液中能大量共存,但通入NO2后会发生化学反应且生成沉淀的一组是( )
| A、Ba2+、Na+、Cl-、HSO3- |
| B、NH4+、K+、ClO-、S2- |
| C、Cu2+、Fe2+、NO3-、SO42- |
| D、Ag+、Na+、NH3?H2O、SO42- |
下列分子式表示的物质一定是纯净物的是( )
| A、CH4 |
| B、C2H6O |
| C、C6H12O6 |
| D、C2H4Cl2 |
在如图所示的装置中,烧瓶中盛有空气,广口瓶中盛放下列物质时可发生喷泉的选项是( )
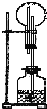

| A、块状大理石和稀硫酸 |
| B、NH4Cl与稀NaOH溶液 |
| C、Na2O2与NaOH溶液 |
| D、铜片与稀盐酸 |
科学的实验方法为我们探索物质世界提供了一把金钥匙.下列实验方法正确的是( )
| A、实验室可通过蒸馏的方法,从含Fe3+的自来水中获得少量纯净水 |
| B、向样品中加入盐酸酸化的氯化钡溶液,以确定样品中是否含有SO42- |
| C、用洁净的玻璃棒蘸取待测液样品溶液置于酒精灯火焰上灼烧,检测是否含有Na+ |
| D、用干燥且洁净的玻璃棒蘸取待测溶液滴在湿润的pH试纸中部,跟标准比色卡对照可测定溶液的pH值 |
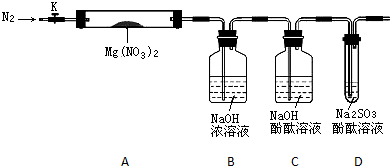

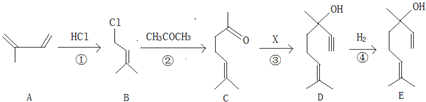
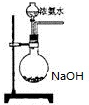 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.