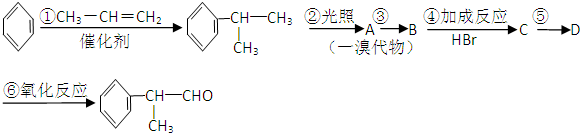
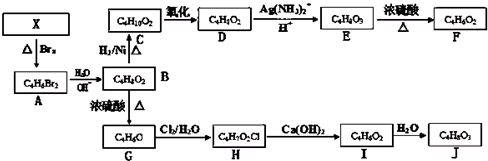
题目内容
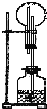
在如图所示的装置中,烧瓶中盛有空气,广口瓶中盛放下列物质时可发生喷泉的选项是( )

| A、块状大理石和稀硫酸 |
| B、NH4Cl与稀NaOH溶液 |
| C、Na2O2与NaOH溶液 |
| D、铜片与稀盐酸 |
考点:性质实验方案的设计
专题:实验题
分析:依据加入的物质能反应产生气体,能导致广口瓶中气压变大,把液体压入烧瓶形成喷泉.
A.考虑硫酸钙的微溶性;
B.考虑氨气的溶解性;
C.过氧化钠和水反应生成氧气;
D.铜和盐酸不反应.
A.考虑硫酸钙的微溶性;
B.考虑氨气的溶解性;
C.过氧化钠和水反应生成氧气;
D.铜和盐酸不反应.
解答:
解:A.CaCO3粉末和稀硫酸反应生成微溶性硫酸钙,阻止反应,不能产生大量二氧化碳,故不能形成喷泉,故A不选;
B.NH4Cl溶液与稀NaOH溶液反应生成氨气溶于水,不能形成喷泉,故B不选;
C.Na2O2与NaOH溶液中水反应生成氧气,导致广口瓶中压强增大,把液体压入广口瓶,故可形成喷泉,故选C;
D.铜片和稀盐酸不反应,不能形成喷泉,故D不选;
故选:C.
B.NH4Cl溶液与稀NaOH溶液反应生成氨气溶于水,不能形成喷泉,故B不选;
C.Na2O2与NaOH溶液中水反应生成氧气,导致广口瓶中压强增大,把液体压入广口瓶,故可形成喷泉,故选C;
D.铜片和稀盐酸不反应,不能形成喷泉,故D不选;
故选:C.
点评:本题考查了喷泉实验,明确形成喷泉的原理是解答的关键,题目难度不大.易错点为A,以为产生二氧化碳,忽落硫酸钙的微溶性.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
在铝中加入某种金属可得到低密度,高强度的新型铝合金,可代替常规的铝合金用于制造航天飞机这种金属是( )
| A、锂 | B、镁 | C、铜 | D、锰 |
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )


| A、加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 |
| B、加热时,②、③中的溶液均变红,冷却后又都变为无色 |
| C、④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D、四个“封管实验”中都有可逆反应发生 |
维生素A1、B2的结构简式分别如图所示:已知: ,下列说法正确的是( )
,下列说法正确的是( )

 ,下列说法正确的是( )
,下列说法正确的是( )
| A、1mol维生素A1最多与溴水中的4molBr2发生加成反应 |
| B、维生素A1的分子式为C19H30O,是一种易溶于水的高分子 |
| C、维生素B2在酸性条件下彻底水解后得到的有机物,其分子内发生酯化得多种酯 |
| D、用-C4H9取代维生素B2苯环上的一个H原子,最多可得4种同分异构体 |
 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.该反应的离子方程式为2MnO4-+5H2C2O4+6H+═2Mn2++10CO2+8H2O.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.该反应的离子方程式为2MnO4-+5H2C2O4+6H+═2Mn2++10CO2+8H2O.设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
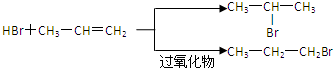
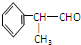 的物质,该物质是一种香料.
的物质,该物质是一种香料.