题目内容
2.在一定条件下,甲苯可生成二甲苯混合物和苯.有关物质的沸点、熔点如表:| 对二甲苯 | 邻二甲苯 | 间二甲苯 | 苯 | |
| 沸点/℃ | 138 | 144 | 139 | 80 |
| 熔点/℃ | 13 | -25 | -47 | 6 |
| A. | 该反应属于取代反应 | |
| B. | 甲苯的沸点高于144℃ | |
| C. | 用蒸馏的方法可将苯从反应所得产物中首先分离出来 | |
| D. | 从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来 |
分析 A、甲苯变成二甲苯是苯环上的氢原子被甲基取代所得,属于取代反应;
B、甲苯的相对分子质量比二甲苯小,沸点比二甲苯低;
C、苯的沸点与二甲苯的沸点相差较大,用蒸馏的方法分离;
D、因为对二甲苯的熔点较高,将温度冷却至-25℃~13℃,对二甲苯形成固体,从而将对二甲苯分离出来.
解答 解:A、甲苯变成二甲苯是苯环上的氢原子被甲基取代所得,属于取代反应,故A正确;
B、甲苯的相对分子质量比二甲苯小,故沸点比二甲苯低,故B错误;
C、苯的沸点与二甲苯的沸点相差较大,可以用蒸馏的方法分离,故C正确;
D、因为对二甲苯的熔点较高,将温度冷却至-25℃~13℃,对二甲苯形成固体,从而将对二甲苯分离出来,故D正确;
故选B.
点评 本题涉及到物质的分离和提纯、有机物的反应类型、沸点高低比较,考查学生根据表格的数据分析解决问题的能力,难度不大.

练习册系列答案
相关题目
12.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,会导致雾霾天气.它主要来自化石燃料的燃烧.下列说法错误的是( )
| A. | 开发风能等洁净能源,减少使用化石燃料 | |
| B. | PM2.5表面积较大易吸附其他物质,对人体危害很大 | |
| C. | 雾霾严重时,中小学生应减少或停止户外活动 | |
| D. | 汽油标准由“国Ⅳ”提到“国 V”后,汽车不再排放氮氧化物 |
13.如图为立方烷的结构简式,其二氯代物有( )
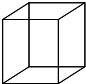

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
10.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 正极反应式为Ag++e-=Ag | |
| C. | 电池放电时Cl-由正极向负极迁移 | |
| D. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ |
17.三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
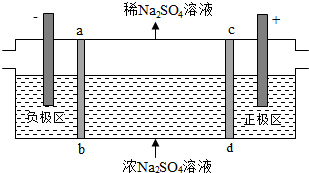

| A. | 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大 | |
| B. | 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品 | |
| C. | 负极反应为2H2O-4e-=O2+4H+,负极区溶液pH降低 | |
| D. | 当电路中通过1mol电子的电量时,会有0.5mol的O2生成 |
7.锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH-+2H2O═2Zn(OH)42-.下列说法正确的是( )
| A. | 充电时,电解质溶液中K+向阳极移动 | |
| B. | 充电时,电解质溶液中c(OH-)逐渐减小 | |
| C. | 放电时,负极反应为:Zn+4OH--2e-═Zn(OH)42- | |
| D. | 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
16.下列有关物质性质的比较顺序中,不正确的是( )
| A. | 微粒半径:Na+>Al3+>S2->Cl- | B. | 沸点:F2<Cl2<Br2<I2 | ||
| C. | 碱性:LiOH<NaOH<KOH<RbOH | D. | 熔点:Li>Na>K>Rb |
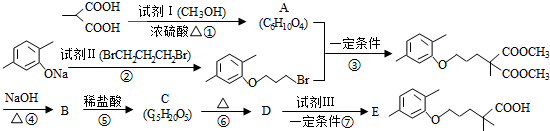
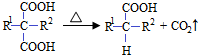 (R1和R2代表烷基)
(R1和R2代表烷基)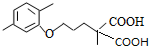 $\stackrel{加热}{→}$
$\stackrel{加热}{→}$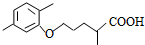 +CO2↑.
+CO2↑.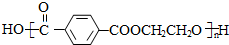 .
.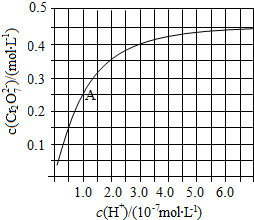 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: