题目内容
COCl2(g) CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
 CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
B
试题分析:化学反应COCl2(g)
 CO(g)+Cl2(g)△H>0,正反应是气体体积增大的吸热反应,①升温平衡向正反应移动,COCl2转化率增大,故①符合;②恒容通入惰性气体,总压增大,反应混合物各组分的浓度不变,平衡不移动,COCl2转化率不变,故②不符合;③增加CO的浓度,平衡向逆反应方向移动,COCl2转化率减小,故③不符合;④减压平衡向正反应方向移动,COCl2转化率增大,故④符合;⑤加催化剂,改变速率不改变平衡,COCl2转化率不变,故⑤不符合;⑥恒压通入惰性气体,压强增大,为保持恒压,体积增大压强减小,平衡正向进行,COCl2转化率增大,故⑥符合,故选:B。
CO(g)+Cl2(g)△H>0,正反应是气体体积增大的吸热反应,①升温平衡向正反应移动,COCl2转化率增大,故①符合;②恒容通入惰性气体,总压增大,反应混合物各组分的浓度不变,平衡不移动,COCl2转化率不变,故②不符合;③增加CO的浓度,平衡向逆反应方向移动,COCl2转化率减小,故③不符合;④减压平衡向正反应方向移动,COCl2转化率增大,故④符合;⑤加催化剂,改变速率不改变平衡,COCl2转化率不变,故⑤不符合;⑥恒压通入惰性气体,压强增大,为保持恒压,体积增大压强减小,平衡正向进行,COCl2转化率增大,故⑥符合,故选:B。
练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
 2SO3(g).某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g).某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是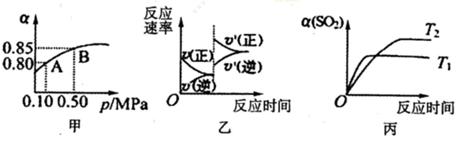
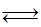 2HI(g) ΔH =" -14.9" kJ/mol,实验时有关数据如下表:
2HI(g) ΔH =" -14.9" kJ/mol,实验时有关数据如下表:
 C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( ) CO(g) + H2O(g),
CO(g) + H2O(g),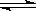 3C(g)+D(g),以下不能说明已达平衡状态的是
3C(g)+D(g),以下不能说明已达平衡状态的是 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是