题目内容
在一定条件下的定容密闭容器中,当物质的下列物理量不再变化时,不能表明反应:A(s)+2B(g) C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( )
 C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( )| A.混合气体的压强 | B.混合气体的密度 |
| C.B的物质的量浓度 | D.混合气体的平均相对分子质量 |
A
试题分析:由于该反应是个反应前后气体体积相等的可逆反应。所以无论反应是否达到平衡,混合气体的压强都不会发生变化。因此不能作为判断平衡的依据。正确。B.由于反应有固体物质参加。若反应未达到平衡,反应正向进行混合气体的质量增大,气体的密度增大;若反应逆向进行,则气体物质的质量减小,气体的密度减小。只有反应达到平衡时,气体的质量和密度才保持不变。因此可以作为反应达到平衡的标志。错误。C.若反应未达到平衡,B的物质的量就会发生变化,B的浓度也会发生改变。因此可以作为判断平衡的标志。错误。 D.由于反应前后气体的物质的量不变,若反应达到平衡,混合气体的质量就不变,气体的平均相对分子质量也不变;若反应未达到平衡,气体的质量就要发生变化 ,气体的摩尔质量或混合气体的平均相对分子质量就要发生变化。因此可以作为判断反应达到平衡的标志。错误。

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
 2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为 ( )
2Z,达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为 ( ) ×100%
×100% ×100%
×100%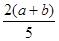 ×100%
×100%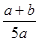 ×100%
×100%

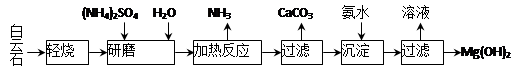
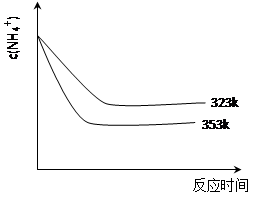
 2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表: 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是 CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是 N2O3 + O2,N2O3
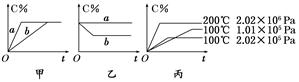
N2O3 + O2,N2O3 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图: