题目内容
下列说法正确的是( )
| A、1molO2和1molN2所占的体积都约为22.4L | ||
B、30% 氨水物质的量浓度为c,稀释至15%后,物质的量浓度比
| ||
| C、等质量的NO2和N2O4所含原子数一定相等 | ||
| D、等体积、等物质的量浓度的强酸溶液中所含的H+离子数一定相等 |
考点:物质的量的相关计算
专题:
分析:A.物质的量一定时,温度、压强会影响气体的体积;
B.氨气的物质的量不变,稀释后溶液质量变为原来的2倍,稀释后溶液密度增大,则溶液体积小于原溶液的2倍,再根据c=
判断;
C.NO2和N2O4中N元素质量分数相等、O元素质量分数相等,二者质量相等,含有原子数目相等;
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数取决于该酸是几元酸.
B.氨气的物质的量不变,稀释后溶液质量变为原来的2倍,稀释后溶液密度增大,则溶液体积小于原溶液的2倍,再根据c=
| n |
| V |
C.NO2和N2O4中N元素质量分数相等、O元素质量分数相等,二者质量相等,含有原子数目相等;
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数取决于该酸是几元酸.
解答:
解:A.物质的量一定时,温度、压强会影响气体的体积,氧气与氮气的温度、压强不确定,不能确定二者体积大小,故A错误;
B.氨气的物质的量不变,稀释后溶液质量变为原来的2倍,稀释后溶液密度增大,则溶液体积小于原溶液的2倍,根据c=
可知,物质的量浓度比
大,故B错误;
C.NO2和N2O4中N、O原子数目之比均为1:2,N元素质量分数相等、O元素质量分数相等,二者质量相等含有原子数目相等,故C正确;
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数取决于该酸是几元酸,如HCl、H2SO4含有氢离子数目不相等,故D错误,
故选C.
B.氨气的物质的量不变,稀释后溶液质量变为原来的2倍,稀释后溶液密度增大,则溶液体积小于原溶液的2倍,根据c=
| n |
| V |
| c |
| 2 |
C.NO2和N2O4中N、O原子数目之比均为1:2,N元素质量分数相等、O元素质量分数相等,二者质量相等含有原子数目相等,故C正确;
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数取决于该酸是几元酸,如HCl、H2SO4含有氢离子数目不相等,故D错误,
故选C.
点评:本题考查物质的量有关计算,难度中等,注意A信息中根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列装置图与对应的叙述相符的是( )
A、 发生的反应为Cu+2Fe3+=Cu2++2Fe2+,X极是负极,Y极的材料也可以是铜 |
B、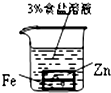 负极反应是Fe-2e-=Fe2+ |
C、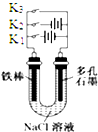 铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>都断开>只闭合K2 |
D、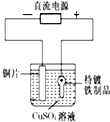 可以实现在铁制品上镀上一层铜 |
下列应用或事实与胶体的性质没有关系的是( )
| A、用明矾净化饮用水 |
| B、可以利用丁达尔效应鉴别胶体和溶液 |
| C、在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 |
| D、清晨的阳光穿过茂密的林木枝叶所产生的美丽的光线 |
下列叙述正确的是( )
| A、只含一种元素的物质,可能为混合物 | ||
| B、非金属元素都是主族元素,最外层电子数都大于或等于3 | ||
C、
| ||
| D、工业由N2制备氨气以及由NH3氧化制备硝酸的过程都属于氮的固定 |
把x mL CO2通过足量的Na2O2后再与y mL NO混合,x与y之和为30.设充分反应后气体的体积缩小为15mL,(不考虑NO2转化为N2O4 ),则x:y可能为( )
①1?:1 ②2?:1 ③5?:4 ④7?:5.
①1?:1 ②2?:1 ③5?:4 ④7?:5.
| A、只有① | B、只有② |
| C、只有③④ | D、①②③④ |
下列叙述正确的是( )
| A、与28 g CO具有相同分子数的CO2的质量一定是44 g |
| B、与V L CO具有相同分子数的CO2,其体积一定是V L |
| C、含有相等氧原子数的CO与CO2,其质量之比为28:11 |
| D、含有相等碳原子数的CO与CO2,其密度之比为21:22 |
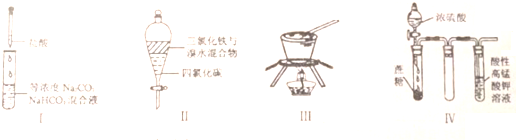 下列由相关图象作出的描述正确的是( )
下列由相关图象作出的描述正确的是( )| A、实验Ⅰ:滴加稀盐酸,NaHCO3先反应立即产生大量气泡 |
| B、实验Ⅱ:振荡后静置分层,上层无色溶液从上口倒出 |
| C、实验Ⅲ:从饱和硫酸钠溶液中提取硫酸钠晶体 |
| D、装置Ⅳ:酸性KMnO4溶液中出现气泡,溶液颜色逐渐褪去 |
某溶液中可能含有Na+、Fe2+、Br-、CO32-、I-、SO32-六种离子中的几种.
(1)取该溶液少量滴加足量氯水后,有气泡产生、溶液呈橙黄色;
(2)向呈橙黄色的溶液中加入氯化钡溶液无沉淀生成;
(3)橙黄色溶液不能使淀粉溶液变蓝.根据上述事实推断,在原溶液中肯定都存在的离子组是( )
(1)取该溶液少量滴加足量氯水后,有气泡产生、溶液呈橙黄色;
(2)向呈橙黄色的溶液中加入氯化钡溶液无沉淀生成;
(3)橙黄色溶液不能使淀粉溶液变蓝.根据上述事实推断,在原溶液中肯定都存在的离子组是( )
| A、Na+、Br-、CO32- |
| B、Na+、I-、SO32- |
| C、Fe2+、I-、SO32- |
| D、Fe2+、Br-、CO32- |
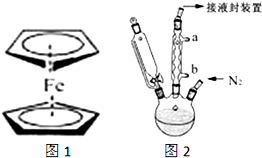 二茂铁(结构如图1)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O
二茂铁(结构如图1)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O