题目内容
下列装置图与对应的叙述相符的是( )
A、 发生的反应为Cu+2Fe3+=Cu2++2Fe2+,X极是负极,Y极的材料也可以是铜 |
B、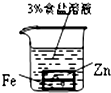 负极反应是Fe-2e-=Fe2+ |
C、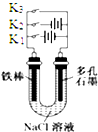 铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>都断开>只闭合K2 |
D、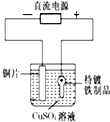 可以实现在铁制品上镀上一层铜 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、Y极材料不能是铜;
B、Zn比Fe活泼,Zn为负极;
C、只闭合K1时,Fe作电解池的阳极,只闭合K3时Fe作原电池的负极,都断开时Fe自然腐蚀,只闭合K2时,Fe作电解池的阴极;
D、铁制品上镀铜,应Cu为阳极,Fe做阴极.
B、Zn比Fe活泼,Zn为负极;
C、只闭合K1时,Fe作电解池的阳极,只闭合K3时Fe作原电池的负极,都断开时Fe自然腐蚀,只闭合K2时,Fe作电解池的阴极;
D、铁制品上镀铜,应Cu为阳极,Fe做阴极.
解答:
解:A、原电池正负极材料不能相同,故A错误;
B、Zn为负极,故B错误;
C、只闭合K1时,Fe作电解池的阳极,只闭合K3时Fe作原电池的负极,都断开时Fe自然腐蚀,只闭合K2时,Fe作电解池的阴极,所以铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>都断开>只闭合K2,故C正确;
D、铁制品上镀铜,应Cu为阳极,Fe做阴极,故D错误;
故选C.
B、Zn为负极,故B错误;
C、只闭合K1时,Fe作电解池的阳极,只闭合K3时Fe作原电池的负极,都断开时Fe自然腐蚀,只闭合K2时,Fe作电解池的阴极,所以铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>都断开>只闭合K2,故C正确;
D、铁制品上镀铜,应Cu为阳极,Fe做阴极,故D错误;
故选C.
点评:本题考查了原电池的构成条件、原电池中正负极确定、金属的腐蚀与防护、电镀,题目难度中等.

练习册系列答案
相关题目
NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是( )
| A、可与硝酸反应 | B、钠的化合物 |
| C、可溶于水 | D、电解质 |
下列关于能源的说法不正确的是( )
| A、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、沼气(主要成分是CH4)是可再生能源 |
| D、太阳能、氢能、风能、地热能、生物质能都是新能源 |
 在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )
在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )| A、在D点,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、在C点,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、在B点,a=12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列盐的溶液蒸干时,能得到原物质的是( )
| A、Na2SO3 |
| B、FeCl3 |
| C、KNO3 |
| D、NH4HCO3 |
常温下,现有NaCl和CuSO4的混合溶液,用Pt电极电解,当电路中通过0.4mol电子的电量时,阴阳两极都产生0.15mol的气体,若电解后溶液体积为10L,则电解后溶液的pH为( )
| A、2 | B、5 | C、9 | D、12 |
在三个密闭容器中分别充入Ar、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
| A、p(H2)>p(O2)>p(Ar) |
| B、p(O2)>p(Ar )>p(H2) |
| C、p(Ar)>p(H2)>p(O2) |
| D、p(H2)>p(Ar)>p(O2) |
下列说法正确的是( )
| A、1molO2和1molN2所占的体积都约为22.4L | ||
B、30% 氨水物质的量浓度为c,稀释至15%后,物质的量浓度比
| ||
| C、等质量的NO2和N2O4所含原子数一定相等 | ||
| D、等体积、等物质的量浓度的强酸溶液中所含的H+离子数一定相等 |