题目内容
下列叙述正确的是( )
| A、与28 g CO具有相同分子数的CO2的质量一定是44 g |
| B、与V L CO具有相同分子数的CO2,其体积一定是V L |
| C、含有相等氧原子数的CO与CO2,其质量之比为28:11 |
| D、含有相等碳原子数的CO与CO2,其密度之比为21:22 |
考点:物质的量与其浓度和气体摩尔体积的综合应用
专题:
分析:根据n=
=
以及ρ=
结合物质的分子构成特点计算.
| m |
| M |
| N |
| NA |
| M |
| Vm |
解答:
解:A.n(CO)=
=1mol,m(CO2)=1mol×44g/mol=44g,故A正确;
B.气体存在的外界条件未知,不能确定体积大小,故B错误;
C.含有相等氧原子数的CO与CO2,物质的量之比为2:1,其质量之比为2×28:44=14:11,故C错误;
D.由ρ=
可知,密度等于相对分子质量之比,为28:44=7:11,故D错误.
故选A.
| 28g |
| 28g/mol |
B.气体存在的外界条件未知,不能确定体积大小,故B错误;
C.含有相等氧原子数的CO与CO2,物质的量之比为2:1,其质量之比为2×28:44=14:11,故C错误;
D.由ρ=
| M |
| Vm |
故选A.
点评:本题综合考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列盐的溶液蒸干时,能得到原物质的是( )
| A、Na2SO3 |
| B、FeCl3 |
| C、KNO3 |
| D、NH4HCO3 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ?mol-,则氢气的标准燃烧热为-241.8 kJ?mol-11 |
| B、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| C、已知2C(s)+2O2(g)=2CO2(g)△H=a2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D、已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
下列化学用语描述中正确的是( )
A、含18个中子的氯原子的核素符号:
| ||
B、比例模型 可以表示CO2 分子或SiO2分子 可以表示CO2 分子或SiO2分子 | ||
| C、HCO3-的电离方程式为:HCO3-+H2O?CO32-+H3O+ | ||
| D、次氯酸的结构式:H-Cl-O |
下列说法正确的是( )
| A、1molO2和1molN2所占的体积都约为22.4L | ||
B、30% 氨水物质的量浓度为c,稀释至15%后,物质的量浓度比
| ||
| C、等质量的NO2和N2O4所含原子数一定相等 | ||
| D、等体积、等物质的量浓度的强酸溶液中所含的H+离子数一定相等 |
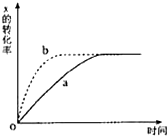 如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进
如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
| A、升高温度 |
| B、加大N的投入量 |
| C、缩小体积 |
| D、加大X的投入量 |