题目内容
18.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图1: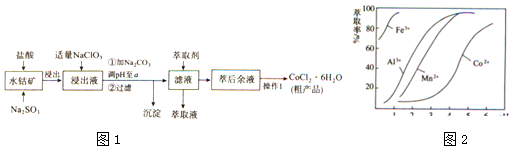
已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
| 淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
分析 含钴废料中加入盐酸和亚硫酸钠,亚硫酸有还原性,Co2O3、Co(OH)3、Fe2O3、Al2O3、MnO和稀盐酸、亚硫酸钠反应生成可溶性的离子,得到的浸出液为CoCl2、AlCl3、FeCl2、MnCl2、NaCl,然后向溶液中加入氯酸钠,可得到FeCl3,然后加入Na2CO3调pH,可得到Fe(OH)3、Al(OH)3沉淀,然后过滤,向滤液中加入萃取剂,将锰离子萃取,萃取后的溶液中主要含有CoCl2,为得到CoCl2•6H2O晶体,将溶液蒸发浓缩、冷却结晶而得到粗产品,据此分析.
解答 解:(1)亚硫酸根离子具有还原性,Co2O3具有氧化性,浸出过程中Co2O3和亚硫酸钠发生氧化还原反应生成硫酸根离子和Co2+,离子方程式为Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;
故答案为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;
(2)NaClO3具有氧化性,能氧化亚铁离子生成铁离子,氯酸根离子被还原生成氯离子,离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;在酸性条件下,NaClO3与氯离子发生氧化还原反应生成氯气,其反应的离子方程式为:ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
故答案为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
(3)惰性电极电解CoCl2溶液,阳极为失电子化合价升高的一极,电极反应式为2Cl--2e-=Cl2↑;
故答案为:2Cl--2e-=Cl2↑;
(4)利用从溶液中制取固体的方法制取氯化钴固体,其操作步骤为:蒸发浓缩、冷却结晶和过滤,
由题可知CoCI2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴,故CoCl2•6H2O在烘干时需减压烘干以降低烘干温度,防止产品分解;
故答案为:蒸发浓缩,冷却结晶;降低烘干温度,防止产品分解.
(5)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子;由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,
故答案为:除去锰离子;B;
(6)根据CoCl2•6H2O的组成分析,造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:1、含有杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大;
故答案为:粗产品含有可溶性氯化物或晶体失去了部分结晶水.
点评 本题通过制取CoCl2•6H2O的工艺流程,考查了物质制备方案的设计,题目难度中等,理解工艺流程图、明确实验操作与设计及相关物质的性质是解答本题的关键,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

| A. | 物质跟氧气反应 | |
| B. | 有氧原子得失的反应 | |
| C. | 有元素化合价升降的反应 | |
| D. | 有电子得失或共用电子对发生偏移的反应 |
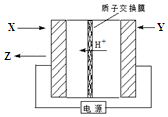 氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )| A. | 图中所示电极中,X端为负极,Y端为正极 | |
| B. | Y参与的电极反应为H2+2e-=2H+ | |
| C. | 反应过程中左边区域溶液pH逐渐升高 | |
| D. | 当有3gH+通过质子交换膜时,Z的体积为11.2L(标况) |
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 除去乙烷中混有的少量乙烯:将混合气体通入足量酸性KMnO4溶液中 | |
| C. | 提取溶解在水中的少量碘:加入CCl4振荡、静置、分层后放出下面有机层再分离 | |
| D. | 检验某溶液中是否含有甲醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热 |
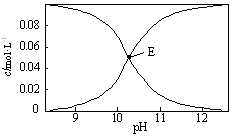 20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )
20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )| A. | pH=9的溶液中:c(HCO3-)>c(H2CO3)>c(CO32-) | |
| B. | c(HCO3-)=c(CO32-)的E点溶液中:c(OH-)+c(CO32-)>c(H+)+c(H2CO3)+0.050 mol•L-1 | |
| C. | pH=11的溶液中:c(Na+)<2c(CO32-)+c(HCO3-) | |
| D. | 0.100 mol•L-1的Na2CO3溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) |
| A. | 对燃煤进行脱硫,减少向大气排放SO2 | |
| B. | 对含SO2、NO2等工业废气进行无害处理后,再排放到大气中 | |
| C. | 为增加工业产值,大力兴建水泥厂、炼钢厂 | |
| D. | 对汽车等交通工具采用清洁燃料,如天然气、甲醇等 |
| A. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,则一定有:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) | |
| B. | 1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 物质的量浓度分别为c1和c2的两种醋酸溶液,若其pH分别为a和a+1,则c1>10c2 |
| A. | 苯和己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | C2H6和C9H20一定互为同系物 | |
| C. | 乙醇与乙酸在加热条件下、由稀硫酸催化可以生成乙酸乙酯 | |
| D. | 新戊烷和异丁烷的一氯代物均为一种 |