题目内容
3.下列说法正确的是( )| A. | 苯和己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | C2H6和C9H20一定互为同系物 | |
| C. | 乙醇与乙酸在加热条件下、由稀硫酸催化可以生成乙酸乙酯 | |
| D. | 新戊烷和异丁烷的一氯代物均为一种 |
分析 A.苯与高锰酸钾不反应;
B.C2H6和C9H20都为烷烃;
C.应用浓硫酸作催化剂;
D.新戊烷有3种H原子,异丁烷中有2种氢原子.
解答 解:A.苯性质稳定,与高锰酸钾不反应,不能使高锰酸钾褪色,故A错误;
B.C2H6和C9H20都为烷烃,二者互为同系物,故B正确;
C.应用浓硫酸作催化剂,加入稀硫酸不反应,故C错误;
D.新戊烷有3种H原子,异丁烷中有2种氢原子,一氯代物分别为3、2种,故D错误.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的组成、结构和性质,难度不大,注意把握有机物的反应条件.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
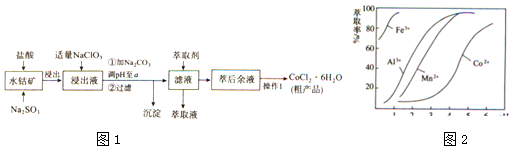
已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
③CoCI2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
| 淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
19.下列对物质的用途描述中错误的是( )
| A. | 明矾可以消毒杀菌常用于净水 | |
| B. | 氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 | |
| C. | 氢氧化铝在医疗上是治疗胃酸过多的一种药剂 | |
| D. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 |
11.下列说法正确的是( )
| A. | 甲烷分子中两个氢原子被氯原子取代后,有两种不同结构分子 | |
| B. | 甲醛能使蛋白质变性,可用于食品防腐剂 | |
| C. | 甲醇分子与水分子之间存在氢键,使甲醇的水溶性显著增强 | |
| D. | 甲苯与苯互为同系物,均能使KMnO4酸性溶液褪色 |
18.在由水电离产生的H+浓度为1×10-13mol•L-1的溶液中,一定能大量共存的离子组是( )
| A. | K+、Cl-、NO3-、S2- | B. | K+、Fe2+、I-、SO42- | ||
| C. | Na+、Cl-、NO3-、SO42- | D. | K+、Ba2+、Cl-、NO3- |
8.下列有关能量的判断或表示方法正确的是( )
| A. | 从C(石墨)=C(金刚石)△H=1.9kJ•mol-1,可知金刚石比石墨更稳定 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | |
| C. | 由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,则向含0.1mol/L的盐酸中加入4.0 gNaOH固体,放出热量等于5.73 kJ | |
| D. | 2 gH2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1 |
12.下列推断不正确的是( )
| A. | 工业上可以用碳还原二氧化硅得到硅和二氧化碳 | |
| B. | 制普通玻璃的主要原料是纯碱、石灰石、石英 | |
| C. | Mg失火不能用CO2灭火;Na失火也不能用CO2灭火 | |
| D. | Fe与S直接化合生成FeS;Al与S也可以直接化合得到Al2S3 |
13.需要有适当的氧化剂才能实现的反应是( )
| A. | FeCl2→FeCl3 | B. | MnO4→Mn2+ | C. | SO3→SO42- | D. | H2O2→H2O |