题目内容
10.常温,下列溶液中各浓度关系不正确的是( )| A. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,则一定有:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) | |
| B. | 1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 物质的量浓度分别为c1和c2的两种醋酸溶液,若其pH分别为a和a+1,则c1>10c2 |
分析 A.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,溶液显碱性,X-离子水解程度大于HX电离程度;
B.1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中铜离子水解、铵根离子水解,铵根离子浓度大于铜离子浓度;
C.溶液中存在电荷守恒分析;
D.弱电解质浓度越小电离度越大,pH越大.
解答 解:A.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,溶液显碱性,X-离子水解程度大于HX电离程度,c(HX)>c(Na+)>c(X-)>c(OH-)>c(H+),故A错误;
B.1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中铜离子水解、铵根离子水解,铵根离子浓度大于铜离子浓度,1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-),故B正确;
C.0.1mol•L-1NaHCO3溶液中电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),c(H2CO3 )>c(CO32-),c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-),故C正确;
D.溶液中存在电荷守恒分析D.弱电解质浓度越小电离度越大,pH越大,而c1α1=10-a,c2α2=10-a-1,α1<α2,所以c1>10 c2,故D正确;
故选A.
点评 本题考查了反应后溶液酸碱性判断、盐类水解、电解质溶液中电荷守恒、物料守恒、弱电解质电离平衡影响因素,题目难度中等.

练习册系列答案
相关题目
20.一般情况下,胶体粒子不易聚集,表现较稳定,主要原因是因为( )
| A. | 胶体有丁达尔效应 | |
| B. | B、胶体粒子直径在1nm-100nm之间 | |
| C. | 胶体粒子很小,不受重力作用 | |
| D. | 同种胶体粒子带同种电荷,它们之间互相排斥 |
1.下列关于胶体的说法不正确的是( )
| A. | 直径为1.3×10-9m 的“钴酞菁”分子分散在水中能形成胶体,则该分子的直径比Na+大 | |
| B. | 煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体 | |
| C. | 丁达尔现象可以用来区别胶体和溶液 | |
| D. | 明矾净水利用了胶体的性质 |
18.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
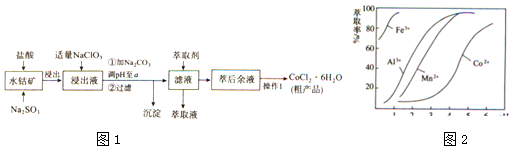
已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
③CoCI2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:
①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表(金属离子浓度为0.01mol/L):
| 淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)惰性电极电解CoCl2溶液的阳极电极反应式为2Cl--2e-=Cl2↑.(注:横坐标依次为1-6;单位PH)
(4)“操作1”中包含3个基本实验操作,它们依次是蒸发浓缩、冷却结晶和过滤.制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是除去锰离子,其使用的最佳pH范围是B.
A. 2.0~2.5B. 3.0~3.5C. 4.0~4.5D. 5.0~5.5
(6)力测定粗产品中CoCl2•H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
5.如图是自然界中N、S两种元素的循环过程:根据图内容,判断下列说法正确的是( )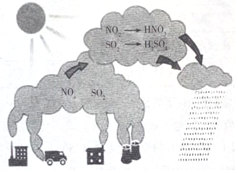

| A. | 图示过程表示了地球臭氧层的破坏过程 | |
| B. | 图中涉及的氧化物均为酸性氧化物 | |
| C. | 机动车尾气含有N的氧化产物 | |
| D. | 图示中描述的过程所涉及的反应均为氧化还原反应 |
15.下列化学反应过程不符合如图关系的是( )
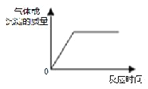

| A. | 向一定量铜片中加入过量浓硝酸 | |
| B. | .向一定量AlCl3溶液通入过量NH3 | |
| C. | .向一定量澄清石灰水中通入过量CO2 | |
| D. | .向一定量MgCl2溶液中滴加过量NaOH |
19.下列对物质的用途描述中错误的是( )
| A. | 明矾可以消毒杀菌常用于净水 | |
| B. | 氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 | |
| C. | 氢氧化铝在医疗上是治疗胃酸过多的一种药剂 | |
| D. | 钠的还原性很强,可以用来冶炼金属钛、锆、铌等 |