题目内容
已知:反应Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.不同温度时K1、K2的值如表:根据表中数据,计算反应CO2(g)+H2(g)?CO(g)+H2O(g)在973K时的平衡常数的K
.
| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
考点:化学平衡的计算
专题:化学平衡专题
分析:Fe(s)+CO2(g)?FeO(s)+CO(g) I、Fe(s)+H2O(g)?FeO(s)+H2(g) II,
将方程式I-II得CO2(g)+H2(g)?CO(g)+H2O(g),则化学平衡常数K=
=
,计算温度为973K时K值.
将方程式I-II得CO2(g)+H2(g)?CO(g)+H2O(g),则化学平衡常数K=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| K1 |
| K2 |
解答:
解:Fe(s)+CO2(g)?FeO(s)+CO(g) I、Fe(s)+H2O(g)?FeO(s)+H2(g) II,
将方程式I-II得CO2(g)+H2(g)?CO(g)+H2O(g),则化学平衡常数K=
=
=
=0.62;
K=0.62;
答:反应CO2(g)+H2(g)?CO(g)+H2O(g)在973K时的平衡常数的K为0.62.
将方程式I-II得CO2(g)+H2(g)?CO(g)+H2O(g),则化学平衡常数K=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| K1 |
| K2 |
| 1.47 |
| 2.38 |
K=0.62;
答:反应CO2(g)+H2(g)?CO(g)+H2O(g)在973K时的平衡常数的K为0.62.
点评:本题考查化学平衡常数的计算等知识点,这些知识点都是高考高频点,知道盖斯定律中化学平衡常数之间的关系式,题目难度中等.

练习册系列答案
相关题目
下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
| 序号 | X | Y | Z | W | 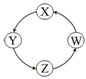 |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A、①②③ | B、①③④ |
| C、②③ | D、①④ |
常温下,0.1mol?L-1的下列溶液中,有关微粒的物质的量浓度关系正确的( )
| A、(NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C、Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| D、NaHCO3溶液:c(Na+)+c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
一定温度下,向aL密闭容器中加入2molNO2(g),发生如下反应:2NO2?2NO+O2,此反应达到平衡状态时的标志是( )
| A、混合气体的颜色变浅 |
| B、混合气体的物质的量相等 |
| C、混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D、单位时间内生成2nmolNO同时生成2nmolNO2 |
下列反应的离子方程式中,正确的是( )
| A、稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ |
| B、稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| C、盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、把金属钠放入水中:Na+2H2O=Na++2OH-+H2↑ |