题目内容
20.在含有I-且能使石蕊试液变红的溶液中能大量共存的离子组为( )| A. | Fe3+、Na+、Br- | B. | NH4+、Na+、AlO2- | C. | Ba2+、Al3+、Cl- | D. | K+、MnO4-、NO3- |
分析 I-具有较强还原性,具有氧化性的离子不能共存;能使石蕊试液变红的溶液呈酸性,溶液中存在大量氢离子,
A.铁离子具有氧化性,能够氧化碘离子;
B.偏铝酸根离子与铵根离子、氢离子反应;
C.三种离子之间不反应,都不与碘离子、氢离子反应;
D.硝酸根离子、高锰酸根离子在酸性条件下能够氧化碘离子.
解答 解:I-具有较强还原性,具有氧化性的离子不能共存;能使石蕊试液变红的溶液呈酸性,溶液中存在大量氢离子,
A.Fe3+能够氧化I-,在溶液中不能大量共存,故A错误;
B.NH4+、H+与AlO2-发生反应,在溶液中不能大量共存,故B错误;
C.Ba2+、Al3+、Cl-之间不反应,都不与碘离子、氢离子反应,在溶液中能够大量共存,故C正确;
D.MnO4-、NO3-在酸性条件下具有强氧化性,能够氧化I-,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于提高学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.将乙烯和氧气的混合气体,用电火花不断引燃,使乙烯完全燃烧(氧气过量).在120℃时测得反应后的混合气体对H2的相对密度是15.75.则原混合气体中乙烯和氧气的体积比为( )
| A. | 1:3 | B. | 1:7 | C. | 1:6 | D. | 5:3 |
15.取碘水四份于试管中,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ,分别加入汽油、CCl4、酒精、NaCl溶液,振荡后静置,现象正确的是( )
| A. | Ⅰ中溶液分层,下层呈紫红色 | B. | Ⅱ中溶液分层,下层呈紫红色 | ||
| C. | Ⅲ中溶液分层,下层呈棕黄色 | D. | Ⅳ中溶液不分层,溶液没有颜色 |
12.关于化学研究的意义,下列说法中正确的是( )
①保证人类的生存:诸如在解决人类粮食、能源、合理使用自然资源以及保护环境方面所作的努力和贡献;
②提高人类的生活质量:诸如合成新的材料,物质的净化和纯化等,均使人类衣、食、住、行的条件有大幅度的改善和提高;
③延长人类的寿命:诸如探明生命过程中的化学奥秘,合成新的药物等.
①保证人类的生存:诸如在解决人类粮食、能源、合理使用自然资源以及保护环境方面所作的努力和贡献;
②提高人类的生活质量:诸如合成新的材料,物质的净化和纯化等,均使人类衣、食、住、行的条件有大幅度的改善和提高;
③延长人类的寿命:诸如探明生命过程中的化学奥秘,合成新的药物等.
| A. | 只有①② | B. | 只有①③ | C. | 只有②③ | D. | ①②③ |
9.下列化学实验操作中,一般情况下不能相互接触的是( )
| A. | 用胶头滴管向试管滴液体时,滴管尖端与试管内壁 | |
| B. | 过滤操作中,漏斗颈与烧杯内壁 | |
| C. | 分液操作中,分液漏斗颈与烧杯内壁 | |
| D. | 过滤操作中,玻璃棒与三层滤纸 |
10.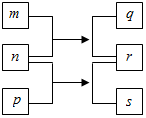 短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )| A. | 离子半径:X>Y>Z | |
| B. | 氧化性:r>m | |
| C. | p和q中均含有离子键 | |
| D. | 等体积等浓度的q溶液与s溶液反应后,溶液呈中性 |