题目内容
4.运用元素周期律分析下面的推断,其中错误的是( )①铍(Be)的氧化物的水化物可能具有两性,②铊(Tl)既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气,③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸,④锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱,⑤硫酸锶(SrSO4)是难溶于水的白色固体,⑥硒化氢(H2Se)是无色,有毒,比H2S稳定的气体.
| A. | ①②③④ | B. | ②④⑥ | C. | ①③⑤ | D. | ②④⑤ |
分析 ①元素周期表中的对角线规则:处于对角线的元素具有相似性;
②同主族元素性质具有相似性和递变性;
③同主族元素性质具有相似性;
④同主族元素性质具有相似性;
⑤同主族元素性质具有相似性;
⑥同主族元素的原子,从上到下氢化物的稳定性逐渐减弱.
解答 解:①铍(Be)的氧化物的水化物和铝的氧化物的水化物氢氧化铝性质相似,可能具有两性,故①正确;
②铊(Tl)和铝同一主族,从上到下,金属性增强,只能和酸液反应放出氢气,Tl(NO3)3溶液应该是中性的,故②误;
③根据卤族元素但只以及银盐的性质,可以推知砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸,故③正确;
④根据钠和锂的性质的递变规律和性质的相似性,可以推知锂(Li)在氧气中剧烈燃烧,产物是Li2O,其溶液是一种强碱,故④错误;
⑤根据第ⅡA元素硫酸盐性质的地变规律,可以知道硫酸锶(SrSO4)是难溶于水的白色固体,故⑤正确;
⑥硒化氢(H2Se)是无色,有毒,不如H2S稳定的气体,故⑥错误.
故选B.
点评 本题考查元素周期表和周期表的综合应用,为高频考点,把握元素的位置、元素的性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
14.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | |
| B. | Cl03- 的空间构型为平面三角形 | |
| C. | SF6中有6对完全相同的成键电子对 | |
| D. | SiF4和SO32- 的中心原子均为sp3杂化 |
12.下列说法中,正确的是( )
| A. | 硅是不活泼的非金属元素,在自然界中可以以游离态的形式存在 | |
| B. | 传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐 | |
| C. | 铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质不活泼 | |
| D. | 铝合金比纯铝的硬度更大、熔点更低 |
9.下列反应中,不属于取代反应的是( )
| A. | 在催化剂存在条件下苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 在催化剂存在条件下,乙烯与氯化氢反应制氯乙烷 | |
| D. | 葡萄糖与银氨溶液反应 |
16.在密闭容器中加入2.0mol SO2和1.0mol O2,一定条件下发生如下反应2SO2+O2?2SO3.反应达到平衡后,各物质的物质的量可能为( )
| n(SO2)/mol | n(O2)/mol | n(SO3)/mol | |
| A | 2.0 | 1.0 | 0 |
| B | 1.0 | 0 | 1.0 |
| C | 0.20 | 0.10 | 1.80 |
| D | 0 | 0 | 2.0 |
| A. | A | B. | B | C. | C | D. | D |
 ;
; ;
;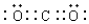 ;
; ;
; ;Na2O2
;Na2O2 ; CO2
; CO2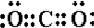 .
.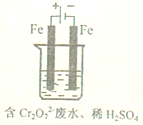 工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.