题目内容
6.A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb(a≠b);C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.(1)元素B、C、D的第一电离能由大到小的顺序为N>O>C (用元素符号表示).
(2)ED3分子的空间构型为平面三角形,中心原子的杂化方式为sp2.
(3)四种分子①BA4②ED3③A2D④CA3键角由大到小排列的顺序是②>①>④>③(填序号).
(4)CA3分子可以与A+离子结合成CA4+离子,这个过程中发生改变的是ac(填序号).
a.微粒的空间构型 b.C原子的杂化类型
c.A-C-A的键角 d.微粒的电子数
(5)EBC-的等电子体中属于分子的有CS2或CO2(填化学式),EBC-的电子式为
 .
.(6)G的价层电子排布式为3d54s1,化合物[G(CA3)6]F3的中心离子的配位数为6.
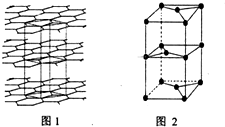
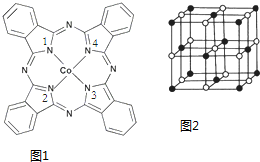
(7)B的某种单质的片层与层状结构如图1所示,其中层间距离为hcm.图2为从层状结构中取出的晶胞.试回答:
①在B的该种单质的片层结构中,B原子数、B-B键数、六元环数之比为2:3:1.
②若B的该种单质中B-B键长为a cm,则B的该种单质的密度为$\frac{16\sqrt{3}}{3h{a}^{2}{N}_{A}}$g•cm-3.
分析 A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb(a≠b),B的最外层电子排布bsbbpb中p轨道有电子,则s轨道一定排满,即b=2,所以B的最外层电子排布2s22p2,则B为C元素;s轨道最多排两个电子,已知a≠b,则a=1,所以A的最外层电子排布为1s1,即A为H元素;C元素对应单质是空气中含量最多的物质,则C为N元素;D的最外层电子数是内层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为O元素;E与D同主族,且位于D的下一周期,则E为S元素;F与E同周期,且是本周期中电负性最大的元素,则F位于第三周期第VIIA族,F为Cl元素;基态G原子核外电子填充在7个能级,且价层电子均为单电子,原子核外电子排布式为1s22s22p63s23p63d54s1,则G为Cr元素.
(1)同周期随原子序数增大,元素第一电离能呈增大趋势,电子排布为全满或半满状态时,原子较稳定,元素的第一电离能较大;
(2)SO3分子中S的孤电子对数=$\frac{1}{2}$×(6-2×3)=0,价层电子对数为3+0=3,S原子杂化轨道数目为3;
(3)孤对电子之间排斥作用大于孤对电子与成键电子层之间的排斥作用,孤对电子与成键电子的排斥力比成键电子之间排斥力大,结合微粒空间构型判断;
(4)NH3分子为三角锥形,键角为107°,NH4+离子为正四面体,键角为109°28′,N原子价层电子对数均为4;
(5)原子总数、价电子总数相同的微粒互为等电子体,与SCN-互为等电子体的分子为CO2等,等电子体微粒的结构相似,SCN-中各原子的连接顺序为S-C-N,S与C形成一对共用电子对,C与N形成三对共用电子对,SCN-得到的一个电子给了S;
(6)Cr的电子排布式为电子排布式为1s22s22p63s23p63d54s1,化合物[Cr(NH3)6]Cl3的中心离子的配位数为6;
(7)①每个碳原子为3个六元环共用,每个碳碳键为2个六元环共用,利用均摊法计算;
②根据均摊法计算晶胞中C原子数目,C-C键长为b pm,则上、下底面为菱形,上底面棱长为a cm×$\frac{\sqrt{3}}{2}$×2=$\sqrt{3}$a cm,石墨的层间距为h cm,则晶胞高为2h cm,计算晶胞质量,根据ρ=$\frac{m}{V}$计算晶胞密度.
解答 解:A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb(a≠b),B的最外层电子排布bsbbpb中p轨道有电子,则s轨道一定排满,即b=2,所以B的最外层电子排布2s22p2,则B为C元素;s轨道最多排两个电子,已知a≠b,则a=1,所以A的最外层电子排布为1s1,即A为H元素;C元素对应单质是空气中含量最多的物质,则C为N元素;D的最外层电子数是内层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为O元素;E与D同主族,且位于D的下一周期,则E为S元素;F与E同周期,且是本周期中电负性最大的元素,则F位于第三周期第VIIA族,F为Cl元素;基态G原子核外电子填充在7个能级,且价层电子均为单电子,原子核外电子排布式为1s22s22p63s23p63d54s1,则G为Cr元素.
(1)同周期随原子序数增大,元素第一电离能呈增大趋势,N元素原子2p能级为半满状态时,原子较稳定,元素的第一电离能大于同周期相邻元素的,所以元素C、N、O的第一电离能由大到小的顺序为N>O>C;
故答案为:N>O>C;
(2)SO3分子中S的孤电子对数=$\frac{1}{2}$×(6-2×3)=0,价层电子对数为3+0=3,则空间构型为平面三角形,的空间构型为平面三角形,中心原子的杂化方式为sp2;
故答案为:平面三角形;sp2;
(3)①CH4为正四面体,②SO3为平面正三角形,键角为120°,③H2O为V形,④NH3为三角锥形,水分子中含有2对孤对电子,氨气电子中含有1对孤对电子,孤对电子之间排斥作用大于孤对电子与成键电子层之间的排斥作用,所以键角由大到小排列的顺序是②>①>④>③;
故答案为:②>①>④>③;
(4)NH3分子为三角锥形,键角为107°,NH4+离子为正四面体,键角为109°28′,N原子价层电子对数均为4,均为sp3杂化,核外电子数均为10,则这个过程中发生改变的是微粒的空间构型和A-C-A的键角;
故答案为:ac;
(5)原子总数、价电子总数相同的微粒互为等电子体,与SCN-互为等电子体的分子为CS2或CO2,SCN-中各原子的连接顺序为S-C-N,S与C形成一对共用电子对,C与N形成三对共用电子对,SCN-得到的一个电子给了S,故SCN-的电子式 ;
;
故答案为:CS2或CO2; ;
;
(6)Cr的电子排布式为电子排布式为1s22s22p63s23p63d54s1,其价层电子排布式为3d54s1;化合物[Cr(NH3)6]Cl3的中心离子的配位数为6;
故答案为:3d54s1;6;
(7)①每个六元环含有C原子个数是6×$\frac{1}{3}$=2,每个C-C被两个环共用,则每个环中含有C-C键数目为6×$\frac{1}{2}$=3,所以C原子数、C-C键数、六元环数之比为2:3:1;
故答案为:2:3:1;
②根据均摊法,晶胞中C原子数目=1+8×$\frac{1}{8}$+4×$\frac{1}{4}$+2×$\frac{1}{2}$=4,晶胞质量为$\frac{4×12}{{N}_{A}}$g,C-C键长为a cm,则上、下底面为菱形,上底面棱长为a cm×$\frac{\sqrt{3}}{2}$×2=$\sqrt{3}$a cm,石墨的层间距为h cm,则晶胞高为2h cm,则晶胞密度为$\frac{4×12}{{N}_{A}}$g÷{[2×$\frac{1}{2}$×$\sqrt{3}$a×$\sqrt{3}$a×sin60°cm]×2h cm}=$\frac{16\sqrt{3}}{3h{a}^{2}{N}_{A}}$ g.cm-3,
故答案为:$\frac{16\sqrt{3}}{3h{a}^{2}{N}_{A}}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、电离能、空间构型与杂化方式判断、价层电子对互斥理论、等电子体、配合物、晶胞计算等,注意对基础知识的理解掌握,(7)为易错点、难点,需要学生具备一定的空间想象与数学计算能力,难度较大.

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案| A. | 碱性溶液中:Rb+、Cs+、CH3COO-、Br- | B. | 饱和溴水中 I-、NO3-、Na+、SO32- | ||
| C. | D+、Cl-、NO3-、SiO32- | D. | Ag+、Fe3+、Br-、SO42- |
| 共价键 | H2分子 | N2分子 | NH3分子 |
| 键能(KJ•mo1-1) | 436 | 945 | 391 |
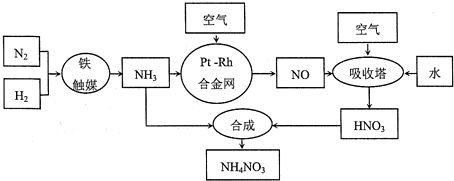
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应. 理论上放出或吸收的热量为Q1,则Q1为93KJ.
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是B
A.Q1>Q2B.Q1<Q2 C.Q1=Q2.

| A. | 硝酸铵、氰化钠、电石和金属钠均属于电解质 | |
| B. | CN-中C元素显+2价,N元素显-3价,则非金属性N>C | |
| C. | 氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡 | |
| D. | 电石属于危化品中的遇湿易燃固体,需贴上右图标志,其着火时不能用水灭火 |
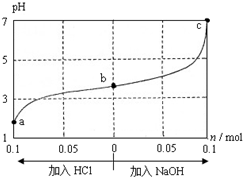
| A. | a、b、c 对应的混合液中,水的电离程度由大到小的顺序的是a>b>c | |
| B. | c点混合液中c(Na+)>c(CH3COO-) | |
| C. | 加入NaOH过程中,$\frac{c(N{a}^{+})×c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| D. | 若忽略体积变化,则25℃时CH3COOH的电离平衡常数 K=$\frac{0.2}{w-0.2}$×10-7 mol•L-1 |
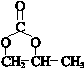 .
.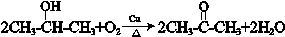 .
.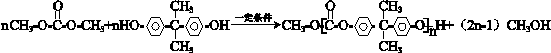 .
.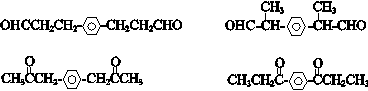 (其中一种).
(其中一种).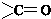 结构
结构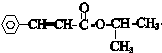 +
+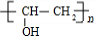 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$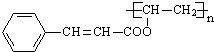 +nCH3CHOHCH3.
+nCH3CHOHCH3.