题目内容
12.化学与科学、技术、社会、环境密切相关,下列说法正确的是( )| A. | 研制乙醇汽油技术,能够降低机动车尾气中有害气体的排放 | |
| B. | 联合制碱法生产纯碱时,在饱和食盐水中先通入二氧化碳,再通入氨气 | |
| C. | 接触法制备硫酸的过程中,在吸收塔内是用大量的水吸收三氧化硫 | |
| D. | 工业上通过电解熔融氧化铝制备金属铝时,常常加入冰晶石作助熔剂 |
分析 A.汽油燃烧产生大量有毒气体;
B.联合制碱生成产纯碱时,先通氨气,再通入二氧化碳;
C.直接用水吸收SO3,易形成酸雾,降低吸收效;
D.铝性质活泼,用电解法制取.
解答 解:A.研制乙醇汽油技术,能够降低机动车尾气中有害气体的排放,有利于环境保护,故A正确;
B.侯氏制碱法的原理就是向饱和的氯化钠溶液里,先通氨气至饱和,再通过量二氧化碳,这样可以保证在碱性条件下生成更多的HCO3-,故B错误;
C.在吸收塔中,直接用水吸收SO3,易形成酸雾,降低SO3吸收效率,应用98.3%硫酸吸收SO3,故C错误;
D.电解熔融Al2O3方法冶炼金属铝时,氧化铝熔点较高,加入冰晶石作熔剂时能降低熔融温度,从而减少能源浪费,故D正确;
故选AD.
点评 本题考查了环境污染与治理、侯氏制碱法原理、工业制硫酸、金属的冶炼,熟悉相关工艺及物质的性质是解题关键,题目难度中等.

练习册系列答案
相关题目
3.以废旧锂电池正极材料(含LiCoO2、Al、Cu、Fe等)为原料通过图1方法获得CoC2O4和Li2CO3.
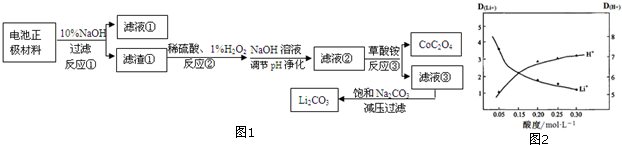
已知:ⅰ.LiCoO2是不溶于水的固体
ⅱ.25℃时,部分电解质的Ksp或Ka
回答下列问题:
(1)滤液①的主要成分是Na[Al(OH)4](填化学式,下同),滤液③中的阴离子除OH-外主要还含有C2O42-、SO42-.
(2)反应②中H2O2改用盐酸代替,不妥的原因是盐酸反应后会产生有毒气体Cl2同时盐酸不能氧化二价亚铁;写出反应②中钴元素化合物与H2O2反应的化学方程式2LiCoO2+3H2SO4+H2O2=2CoSO4+O2↑+Li2SO4+4H2O.
(3)减压过滤就是抽滤,抽滤操作与普通过滤相比,除了得到沉淀较干燥外,还有一个优点是过滤速度快.
(4)若滤液②中c(Co2+)=3.0mol•L-1,加入等体积的(NH4)2C2O4后,钴的沉降率达到99.9%,计算滤液③中 c(C2O42-)=4.2×10-5mol•L-1.
(5)采用有机物萃取Li+的方法可提取锂.其中有机物中加入一定量Fe3+以提高萃取率,D为离子在有机层与水层的分配比.图2是其他条件不变,水相的酸度与D(H+)、D(Li+)的变化图象.解释萃取液酸度控制在0.05mol•L-1的原因可抑制萃取剂中Fe3+水解,同时此酸度时,Li+的萃取率较高.(写2点)
(6)在反应③中用草酸铵作沉淀剂,25℃时,(NH4)2C2O4溶液pH<7(填“=”或“>”或“<”).

已知:ⅰ.LiCoO2是不溶于水的固体
ⅱ.25℃时,部分电解质的Ksp或Ka
| 弱电解质 | CoC2O4 | Fe(OH)3 | NH3•H2O | H2C2O4 |
| 平衡常数 | Ksp=6.3×10-8 | Ksp=2.79×10-39 | Ka=1.7×10-5 | Ka1=5.6×10-2 Ka2=5.4×10-5 |
(1)滤液①的主要成分是Na[Al(OH)4](填化学式,下同),滤液③中的阴离子除OH-外主要还含有C2O42-、SO42-.
(2)反应②中H2O2改用盐酸代替,不妥的原因是盐酸反应后会产生有毒气体Cl2同时盐酸不能氧化二价亚铁;写出反应②中钴元素化合物与H2O2反应的化学方程式2LiCoO2+3H2SO4+H2O2=2CoSO4+O2↑+Li2SO4+4H2O.
(3)减压过滤就是抽滤,抽滤操作与普通过滤相比,除了得到沉淀较干燥外,还有一个优点是过滤速度快.
(4)若滤液②中c(Co2+)=3.0mol•L-1,加入等体积的(NH4)2C2O4后,钴的沉降率达到99.9%,计算滤液③中 c(C2O42-)=4.2×10-5mol•L-1.
(5)采用有机物萃取Li+的方法可提取锂.其中有机物中加入一定量Fe3+以提高萃取率,D为离子在有机层与水层的分配比.图2是其他条件不变,水相的酸度与D(H+)、D(Li+)的变化图象.解释萃取液酸度控制在0.05mol•L-1的原因可抑制萃取剂中Fe3+水解,同时此酸度时,Li+的萃取率较高.(写2点)
(6)在反应③中用草酸铵作沉淀剂,25℃时,(NH4)2C2O4溶液pH<7(填“=”或“>”或“<”).
20.下列有关胶体的说法错误的是( )
| A. | 胶粒可以透过滤纸,不能透过半透膜 | |
| B. | 采用喷雾型药剂形成一定大小的液珠,可有效提高药物疗效 | |
| C. | 冶金工业的矿粒除尘利用了丁达尔效应 | |
| D. | 空气中的雾压现象体现了胶体的存在 |
17.下列离子方程式书写错误的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2H2O+2OH-═2AlO2-+3H2↑ | |
| B. | Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
4.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 密度:苯<水<溴苯 | B. | 沸点:戊烷>2-甲基丁烷>丙烷 | ||
| C. | 酸性:HCO3-<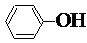 <H2CO3 <H2CO3 | D. | 与Na反应的速率:水>苯酚>乙醇 |
8.根据表中7种短周期元素的有关信息判断,下列说法错误的是( )
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 |
| A. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 | |
| B. | 元素②氢化物的沸点小于元素⑤氢化物的沸点 | |
| C. | 元素②⑥形成的化合物具有两性 | |
| D. | ⑦①可形成离子化合物 |

 CH2-CHCl
CH2-CHCl .
.


