题目内容
11.关于下列实验说法正确的是( )A、利用该装置准确量取9.20ml硫酸溶液 | B、将洗涤液转移到容量瓶中,应该采取如图的操作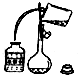 |
| C、过滤和蒸发中都需要使用玻璃棒,且玻璃棒的用途一样 | D、保存NaOH应使用带橡皮塞的玻璃试剂瓶 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.量筒精确到0.1ml;
B.容量瓶不能直接配制溶液;
C.在过滤时,用玻璃棒引流;在蒸发过程中,用玻璃棒搅拌,使液体均匀受热;
D.氢氧化钠溶液能够与二氧化硅反应.
解答 解:A.量筒精确到0.1ml,无法量取9.20mL水,故A错误;
B.容量瓶不能直接配制溶液,应现在小烧杯中稀释,故B错误;
C.在过滤时,用玻璃棒引流;在蒸发过程中,用玻璃棒搅拌,使液体均匀受热,防止液体飞溅,故C错误;
D.玻璃的主要成分为二氧化硅,氢氧化钠溶液能够与二氧化硅反应,不能用带玻璃塞的试剂瓶盛放氢氧化钠溶液,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及仪器的使用、转移液体、物质制备及分离与提纯以及保存等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
9.一定温度下,向容积恒定的密闭容器中投入1mol A和1mol B,发生如下可逆反应:2A(g)+B(g)═C(g)+D(s),达到平衡时,测得压强为原压强的四分之三.则B的转化率为( )
| A. | 25% | B. | 40% | C. | 50% | D. | 75% |
2. (1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
(1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)?CO2(g)+H2(g);△H<0 CO和H2O浓度变化如图,则0~4min的平均反应速率v(H2O)=0.03mol/(L•min);
(2)该反应的化学平衡常数表达式K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.
T℃时物质浓度(mol/L)的变化
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.表中3min~4min 时间段之间反应处于平衡状态.
 (1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
(1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0 CO和H2O浓度变化如图,则0~4min的平均反应速率v(H2O)=0.03mol/(L•min);
(2)该反应的化学平衡常数表达式K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.
T℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
16.有FeO、Fe3O4 的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原固体混介合物减轻了0.8g,将等质量的原混合物与硫酸反应,欲使之完全溶解,需0.5mol•L-1的硫酸的体积至少为( )
| A. | 0.1L | B. | 0.2L | C. | 0.4L | D. | 0.5L |
3.元素的种类和原子的种类相比较( )
| A. | 前者多 | B. | 后者多 | C. | 相等 | D. | 不能确定 |
20.在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐”(BrO3-)这一潜在致癌物质被做了严格限制.有关专家解释,矿泉水在开采过程中会含有少量溴化物(O3),在后续的生产过程中经臭氧(O3)处理逐渐转化为溴酸盐.下列有关该转化过程的认识正确的是( )
| A. | 该过程中溴化物(Br-)得到电子 | |
| B. | 该过程中溴元素被还原,氧元素被氧化 | |
| C. | 该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 | |
| D. | 该过程中溴元素发生氧化反应,氧元素发生还原反应 |
1.某混合溶液中所含离子的浓度如下表,则Mn+及a值可能为( )
| 所含离子 | NO${\;}_{3}^{-}$ | SO${\;}_{4}^{2-}$ | H+ | Na+ | Mn+ |
| 浓度(mol/L) | 3 | 1 | 2 | 1 | a |
| A. | Mg2+、1 | B. | Ba2+、0.5 | C. | Al3+、1.5 | D. | Fe2+、2 |
