题目内容
1.某混合溶液中所含离子的浓度如下表,则Mn+及a值可能为( )| 所含离子 | NO${\;}_{3}^{-}$ | SO${\;}_{4}^{2-}$ | H+ | Na+ | Mn+ |
| 浓度(mol/L) | 3 | 1 | 2 | 1 | a |
| A. | Mg2+、1 | B. | Ba2+、0.5 | C. | Al3+、1.5 | D. | Fe2+、2 |
分析 由电荷守恒计算n,再结合离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应来解答.
解答 解:由电荷守恒可知,
3×1+1×2=2×1+1×1+n×a,
解得na=2,
由选项中的离子可知,则n只能为2,则a=1,
且Fe2+、H+、NO3-发生氧化还原反应不能共存,
Ba2+、SO42-结合生成沉淀,不能大量共存,
故选A.
点评 本题考查离子的共存,为高频考点,把握电荷守恒及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应为解答的难点,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
11.关于下列实验说法正确的是( )
A、利用该装置准确量取9.20ml硫酸溶液 | B、将洗涤液转移到容量瓶中,应该采取如图的操作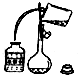 |
| C、过滤和蒸发中都需要使用玻璃棒,且玻璃棒的用途一样 | D、保存NaOH应使用带橡皮塞的玻璃试剂瓶 |
| A. | A | B. | B | C. | C | D. | D |
13.下列反应的离子方程式正确的是( )
| A. | AgNO3溶液中滴入少量的NaHS溶液:2Ag++S2-=Ag2S↓ | |
| B. | 将相互接触的铜片和锌片置于稀硫酸中,铜片表面有气泡产生:Cu+2H+═Cu2++H2↑ | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| D. | 硫酸铝溶液与纯碱溶液混合:2Al3++3CO32-=2Al(OH)3↓+3CO2↑ |
10.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 25℃,1.01×105Pa,22.4LSO2中含有的原子数为3NA | |
| B. | 1 mol S2-中的电子数为18NA | |
| C. | 7.8gNa2O2加入足量的水中,转移的电子数为0.2NA | |
| D. | 在标准状况下,各为l mol的二氧化硫、CCl4的体积均约为22.4L |
11.下列反应的离子方程式正确的是( )
| A. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O | |
| B. | 稀盐酸除铁锈:6H++Fe2O3=2Fe3++3H2O | |
| C. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |


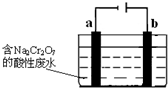 工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而被除去.如图为电解装置示意图(电极材料分别为铁和石墨):
工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而被除去.如图为电解装置示意图(电极材料分别为铁和石墨):
 .
. .
. .
.