题目内容
20.在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐”(BrO3-)这一潜在致癌物质被做了严格限制.有关专家解释,矿泉水在开采过程中会含有少量溴化物(O3),在后续的生产过程中经臭氧(O3)处理逐渐转化为溴酸盐.下列有关该转化过程的认识正确的是( )| A. | 该过程中溴化物(Br-)得到电子 | |
| B. | 该过程中溴元素被还原,氧元素被氧化 | |
| C. | 该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 | |
| D. | 该过程中溴元素发生氧化反应,氧元素发生还原反应 |
分析 由题中信息可知,反应物为Br-和O3,生成物为BrO3-,说明Br-被氧化生成BrO3-,从化合价的角度分析.
解答 解:A.Br-被氧化生成BrO3-,该过程中溴化物(Br-)失去电子,故A错误;
B.该过程中氧元素被还原,溴元素被氧化,故B错误;
C.氧化剂为O3,还原剂为Br-,故C错误;
D.从化合价的变化可知,该过程中溴元素发生氧化反应,氧元素发生还原反应,故D正确.
故选D.
点评 本题考查氧化还原反应,题目难度不大,本题注意加强对氧化还原反应有关概念的理解,把握氧化还原反应的特征.

练习册系列答案
相关题目
11.关于下列实验说法正确的是( )
A、利用该装置准确量取9.20ml硫酸溶液 | B、将洗涤液转移到容量瓶中,应该采取如图的操作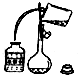 |
| C、过滤和蒸发中都需要使用玻璃棒,且玻璃棒的用途一样 | D、保存NaOH应使用带橡皮塞的玻璃试剂瓶 |
| A. | A | B. | B | C. | C | D. | D |
8.下列有关NaHSO3溶液的叙述正确的是( )
| A. | 该溶液中,K+、Ca2+、Cl2、Br-可以大量共存 | |
| B. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具漂白性 | |
| C. | 与FeCl3反应的离子方程式:SO32-+2Fe3++H2O=SO42-+2Fe2++2H+ | |
| D. | 和足量Ca(OH)2溶液反应的离子方程式:Ca2++OH-+HSO3-=CaSO3↓+H2O |
15.下列关于物质性质的叙述中,正确的是( )
| A. | Cl2能与金属活动性顺序表中大多数金属发生化学反应 | |
| B. | N2是大气的主要成分之一,雷雨时,可直接转化为NO2 | |
| C. | 硫是一种淡黄色的能溶于水的晶体,只有氧化性 | |
| D. | 某气体通入澄清石灰水有白色沉淀产生,该气体一定是CO2 |
5.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℉、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| D. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应△H=+2×283.0 kJ•mol-1 |
10.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 25℃,1.01×105Pa,22.4LSO2中含有的原子数为3NA | |
| B. | 1 mol S2-中的电子数为18NA | |
| C. | 7.8gNa2O2加入足量的水中,转移的电子数为0.2NA | |
| D. | 在标准状况下,各为l mol的二氧化硫、CCl4的体积均约为22.4L |

