题目内容
14.常温下,下列盐溶液 pH<7的是( )| A. | NaHCO3溶液 | B. | NaHSO3溶液 | C. | CH3COONa溶液 | D. | Na2HPO4溶液 |
分析 常温下,pH=7的溶液呈中性,pH>7的溶液呈碱性,pH<7的溶液呈酸性,常温下盐溶液pH<7,说明该盐溶液呈酸性,根据这几种钠盐类型确定溶液酸碱性.
解答 解:A.碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子电离程度小于水解程度导致溶液呈碱性,pH>7,故A错误;
B.亚硫酸氢钠是强碱弱酸酸式盐,亚硫酸氢根离子电离程度大于水解程度导致溶液呈酸性,则pH<7,故B正确;
C.醋酸钠是强碱弱酸盐,醋酸根离子水解导致溶液呈碱性,pH>7,故C错误;
D.磷酸氢二钠是强碱弱酸酸式盐,磷酸氢根离子电离程度小于其水解程度导致溶液呈碱性,pH>7,故D错误;
故选B.
点评 本题考查溶液酸碱性判断,为高频考点,侧重考查学生分析判断能力,明确酸式酸根离子水解程度与其电离程度关系是解本题关键,注意AB区别,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
4.下列说法正确的是( )
| A. | 在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 | |
| B. | 放热反应中,反应物的总能量大于生成物的总能量 | |
| C. | 放热反应发生时不一定要加热,但吸热反应必须要加热才能发生 | |
| D. | 断开化学键的过程会放出能量 |
5.下列关于胶体的叙述不正确的是( )
| A. | 将1mL饱和氯化铁溶液逐滴加入到20mL温水中,边加边搅拌 | |
| B. | 向Fe(OH)3胶体中加入少量H2SO4溶液,会生成红褐色沉淀 | |
| C. | 可利用丁达尔效应区分胶体和溶液 | |
| D. | 胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 |
9.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 无色溶液:Ca2+、H+、Cl-、HSO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、NO3-、I-、AlO2- | |
| C. | FeCl3溶液:K+、Na+、Fe2+、S2- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
19.下列药品,在空气中既不易被氧化,也不易分解,且可以用无色玻璃瓶存放的是( )
| A. | 氯水 | B. | 钠 | C. | 浓硝酸 | D. | 浓盐酸 |
6.在酸性溶液中能大量共存而且溶液为无色透明的是( )
| A. | Na+、Al3+、SO42-、NO3- | B. | K+、Na+、SO42-、Ba2+ | ||
| C. | K+、MnO4-、NH4+、Cl- | D. | Cu2+、K+、HCO3-、NO3- |
10.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
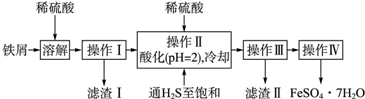
查询资料,得有关物质的相关数据如表:
(1)操作Ⅱ中,通入硫化氢至饱和的目的是除去溶液中的Sn2+;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀,并防止Fe2+被氧化.
(2)滤渣Ⅱ的主要成分是SnS.
(3)操作Ⅳ得到的绿矾晶体用少量冰水此空删去洗涤,其目的是:此空删去
①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.010 00mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①滴定时盛放KMnO4溶液的仪器为酸式滴定管(填仪器名称).
②判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色.
③计算上述样品中FeSO4•7H2O的质量分数为97.5%.

| 25℃时 | pH[] |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)操作Ⅱ中,通入硫化氢至饱和的目的是除去溶液中的Sn2+;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀,并防止Fe2+被氧化.
(2)滤渣Ⅱ的主要成分是SnS.
(3)操作Ⅳ得到的绿矾晶体用少量冰水此空删去洗涤,其目的是:此空删去
①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.010 00mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①滴定时盛放KMnO4溶液的仪器为酸式滴定管(填仪器名称).
②判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色.
③计算上述样品中FeSO4•7H2O的质量分数为97.5%.