题目内容
5.下列表示方法正确的是( )| A. | HCl的电子式为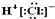 | B. | N2的结构式 N≡N | ||
| C. | O原子处于基态的轨道表示式: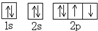 | D. | 用电子式表示MgCl2的形成: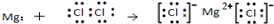 |
分析 A.氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子;B.氮气中存在N、N三键;C.O原子最外层有6个电子;D.氯化镁为离子化合物,据此书写形成过程.
解答 解:A.氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为 ,故A错误;B.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为
,故A错误;B.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为 ,结构式为N≡N,故B正确;C.根据原子核外电子排布原则:电子优先单独占据1个轨道,且自旋方向相同.故C错误;D.用电子式表示物质的形成过程时,箭头左方应写出原子的电子式,右方写出物质的电子式,故D错误.
,结构式为N≡N,故B正确;C.根据原子核外电子排布原则:电子优先单独占据1个轨道,且自旋方向相同.故C错误;D.用电子式表示物质的形成过程时,箭头左方应写出原子的电子式,右方写出物质的电子式,故D错误.
故选B.
点评 本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
15.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.Z的+2价阳离子电子层结构与氖相同,X、M同主族,Y在同周期主族元素中原子半径最大.Y和M可以形成Y2M型化合物.下列有关说法正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的酸性:N>M | |
| C. | 单质与水反应的剧烈程度:Z>Y | |
| D. | 气态氢化物稳定性:M>X |
16.有机化合物9,10-二甲基菲的结构如图所示.其苯环上七氯代物的同分异构体有( )
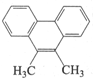

| A. | 8种 | B. | 5种 | C. | 4种 | D. | 3种 |
13.某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品可能是( )
| A. | 乙二醇 | B. | 乙醇 | C. | 乙醛 | D. | 丙三醇 |
20.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | O.lmol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| B. | 分子数目为0.1NA的N2和NH3混合气体,原子间含有的共用电子对数为0.3NA | |
| C. | 电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA | |
| D. | 常温常压下,4.4g乙醛所含σ键数目为0.7NA |
10.下列反应可以设计成原电池的是( )
①CaO+H2O═Ca(OH)2
②Fe+H2SO4═FeSO4+H2↑
③2H2O═2H2↑+O2↑
④NaCl+AgNO3═AgCl↓+NaNO3
⑤Cu+2AgNO3═2Ag+Cu(NO3)2
⑥Fe+2FeCl3═3FeCl2.
①CaO+H2O═Ca(OH)2
②Fe+H2SO4═FeSO4+H2↑
③2H2O═2H2↑+O2↑
④NaCl+AgNO3═AgCl↓+NaNO3
⑤Cu+2AgNO3═2Ag+Cu(NO3)2
⑥Fe+2FeCl3═3FeCl2.
| A. | ①②④⑤⑥ | B. | ②③⑤⑥ | C. | ②⑤⑥ | D. | 全部 |
17.以下说法正确的是( )
| A. | 电子在原子核外排布时,总是尽先排在能量最高的电子层里 | |
| B. | 原子核外各电子层最多能容纳的电子数2n2,所以钾原子的M层有9个电子 | |
| C. | 稀有气体元素都形成了稳定的电子层结构,所以这些元素一定不存在化合态 | |
| D. | 在1~18号元素中,最外层电子数等于电子层数的元素有3种 |
14.下列有关原电池的说法中正确的是( )
| A. | 在外电路中,电子由负极流向正极 | |
| B. | 在内电路中,电子由正极流向负极 | |
| C. | 原电池工作时,正极表面一定有气泡产生 | |
| D. | 原电池工作时,一定不会伴随着热能变化 |
15.下列物质的电子式书写正确的是( )
| A. | Na2O Na${\;}_{2}^{+}$[${\;}_{×}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{×}^{•}$]2- | |
| B. | H2S H+[${\;}_{×}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{×}^{•}$]2-H+ | |
| C. | H2O2 H${\;}_{×}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{×}^{•}$H | |
| D. | N2 N${\;}_{•}^{•}$${\;}_{•}^{•}$${\;}_{•}^{•}$N |