题目内容
15.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.Z的+2价阳离子电子层结构与氖相同,X、M同主族,Y在同周期主族元素中原子半径最大.Y和M可以形成Y2M型化合物.下列有关说法正确的是( )| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的酸性:N>M | |
| C. | 单质与水反应的剧烈程度:Z>Y | |
| D. | 气态氢化物稳定性:M>X |
分析 X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,Z的+2价阳离子电子层结构与氖相同,故Z为Mg元素;Y在同周期主族元素中原子半径最大,则Y处于IA则,由原子序数可知M、N处于第三周期,且族序数Mg<M<N,X、M同主族,则X、M的族序数大于ⅡA族,而Y的原子序数又大于Z、小于Mg,可推知Y为Na;Y和M可以形成Y2M型化合物,则M表现-2价,故M为S元素、X为O元素;N的原子序数大于硫,故N为Cl.
解答 解:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,Z的+2价阳离子电子层结构与氖相同,故Z为Mg元素;Y在同周期主族元素中原子半径最大,则Y处于IA则,由原子序数可知M、N处于第三周期,且族序数Mg<M<N,X、M同主族,则X、M的族序数大于ⅡA族,而Y的原子序数又大于Z、小于Mg,可推知Y为Na;Y和M可以形成Y2M型化合物,则M表现-2价,故M为S元素、X为O元素;N的原子序数大于硫,故N为Cl.
A.X为O元素,Y为Na元素,二者可以形成Na2O、Na2O2,故A错误;
B.同周期自左而右非金属性增强,最高价氧化物对应水化物的酸性最强,故酸性:高氯酸>硫酸,故B正确;
C.同周期自左而右金属性减弱,故金属性Na>Mg,单质与水反应的剧烈程度:Na>Mg,故C错误;
D.同主族自上而下非金属性减弱,气态氢化物稳定性减弱,故气态氢化物稳定性X>M,故D错误;
故选B.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重考查学生分析推理能力以及元素周期律,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5. 溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr$\stackrel{硫酸}{→}$CH3CH2Br+H2O
某课外小组欲在实验室制备溴乙烷的装置如图.数据如下表.
请回答下列问题.
(1)加入药品之前须做的操作是:检查装置的气密性,实验进行的途中若发现未加入碎瓷片,其处理的方法是待冷却后重新进行操作.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是冷凝回流.温度计的温度应控制在38.4℃~78.5℃之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是SO2+2OH-=SO32-+H2O,Br2+2OH-=Br-+BrO-+H2O,此操作可在分液漏斗(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了防止溴化氢气体的挥发.
(5)粗产品中含有的主要有机液体杂质是乙醚,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行蒸馏操作.
 溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr$\stackrel{硫酸}{→}$CH3CH2Br+H2O
某课外小组欲在实验室制备溴乙烷的装置如图.数据如下表.
| 物质 数据 | 乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 浓硫酸 |
| 密度/g•cm-3 | 0.79 | 1.46 | 2.2 | 0.71 | 1.84 |
| 熔点(℃) | -130 | -119 | 9 | -116 | 10 |
| 沸点(℃) | 78.5 | 38.4 | 132 | 34.6 | 338 |
| 在水中的溶解度(g/100g水) | 互溶 | 0.914 | 1 | 7.5 | 互溶 |
(1)加入药品之前须做的操作是:检查装置的气密性,实验进行的途中若发现未加入碎瓷片,其处理的方法是待冷却后重新进行操作.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是冷凝回流.温度计的温度应控制在38.4℃~78.5℃之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是SO2+2OH-=SO32-+H2O,Br2+2OH-=Br-+BrO-+H2O,此操作可在分液漏斗(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了防止溴化氢气体的挥发.
(5)粗产品中含有的主要有机液体杂质是乙醚,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行蒸馏操作.
6.下列离子方程式正确的是( )
| A. | 醋酸溶液与氢氧化铜反应:2CH3COOH+Cu(OH)2 Cu2++2CH3COO-+2H2O | |
| B. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO32- | |
| D. | 甲酸溶液与足量的银氨溶液共热HCOOH+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
3.提纯或分离下列混合物,所选用的试剂或方法不正确的是( )
| A. | 分离汽油和氯化钾溶液的混合液,采用分液的方法 | |
| B. | 除去NaCl溶液中混有的I2,用酒精把NaCl溶液中的I2萃取出来 | |
| C. | 除去02中混有的水蒸气,通过盛有浓硫酸的洗气瓶洗气 | |
| D. | 除去固体碘中混有的少量 Nal.采用加热升华的方法 |
20.把X、Y、Z三种金属分别浸入相同质量分数的稀硫酸中,Y表面有气泡产生,X、Z表面无明显变化;把Z金属浸入X的硝酸盐溶液中,Z表面析出X.则三种金属的活动性顺序由强到弱的是( )
| A. | Y、Z、X | B. | X、Y、Z | C. | X、Z、Y | D. | Z、Y、X |
7.磷和氮同为VA族元素,它们对应的化合物在结构上和性质上有许多相似之处.下列对PH4I的说法中,不正确的是( )
| A. | 它是离子化合物 | B. | 它的热稳定性好 | ||
| C. | 它能与强碱发生反应 | D. | 其溶液可与AgNO3溶液发生反应 |
4.将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热一段时间后,溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是( )
| A. | n(Na+):n(Cl-)可能为7:3 | |
| B. | 与NaOH反应的氯气一定为0.3mol | |
| C. | 当转移电子为n mol时,则0.15<n<0.25 | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为6:1:1 |
5.下列表示方法正确的是( )
| A. | HCl的电子式为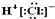 | B. | N2的结构式 N≡N | ||
| C. | O原子处于基态的轨道表示式: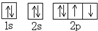 | D. | 用电子式表示MgCl2的形成: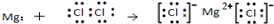 |
 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题: