题目内容
11.设NA为阿伏加德罗常数,下列叙述正确的是( )| A. | 2L 1mol/L过氧化氢溶液中含氧原子数为4NA | |
| B. | 6.8g熔融的KHSO4中含有0.1NA个阳离子 | |
| C. | 2mol MnO2与足量的浓盐酸加热充分反应,转移电子数为4NA | |
| D. | 密闭容器中2molNO2和1molO2充分反应,产物分子数为2NA |
分析 A.溶液中含氧原子的有过氧化氢和水;
B.熔融硫酸氢钾电离出钾离子和硫酸氢根离子;
C.2mol MnO2与足量的浓盐酸加热充分反应,结合二氧化锰物质的量和转移电子之间的关系式计算;
D.NO2和N2O4之间存在转化,方程式2NO2?N2O4.
解答 解:A.水中也含氧原子,2L 1mol/L过氧化氢溶液中含氧原子数大于4NA,故A错误;
B.6.8g熔融的KHSO4的物质的量0.05mol,0.05mol熔融硫酸氢钾能够电离出0.05mol钾离子和0.05mol硫酸氢根离子,所以含有的阳离子数为0.05NA,故B错误;
C.二氧化锰和转移电子之间的关系式知,转移电子个数=2mol×(4-2)×NA/mol=4 NA,故C正确;
D.NO和O2反应方程式为2NO+O2=2NO2,根据方程式知,2molNO与1molO2恰好完全反应生成2molNO2,但NO2和N2O4之间存在转化,方程式2NO2?N2O4,所以产物分子数小于2NA,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的综合应用,熟练掌握物质的量与阿伏伽德罗常数、氧化还原反应电子转移计算、物质结构等是解题关键,注意过氧化氢溶液中水的存在,题目难度中等.

练习册系列答案
相关题目
2.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4L NO与11.2L O2混合充分反应,产物的分子数为NA | |
| B. | 14g乙烯和丙烯混合气体中含有C-H共价键的数目为2NA | |
| C. | l mol Cu与足量的硫充分反应,电子转移数为2NA | |
| D. | 100mL l mol•L-1KClO溶液中,阴离子的数目小于0.1NA |
19.用NA表示阿伏加徳罗常数的数值,下列判断正确的是( )
| A. | 常温常压下,22.4 L CO2含有的分子数为NA | |
| B. | 1mol•L-1的Ba(OH)2溶液中含有的氢氧根离子数目为2NA | |
| C. | 常温常压下,18 g H2O含有的氢原子数为2NA | |
| D. | 1mol Fe在足量的Cl2中充分燃烧,转移的电子数为2NA |
6.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1molCH3+所含的电子数为9NA | |
| B. | 标准状况下,11.2 L HF的分子数为0.5NA | |
| C. | 39 g Na2O2与足量水反应,转移电子数为NA | |
| D. | 1 mol乙醇中含有共用电子对数为8NA |
16.下列说法正确的是( )
| A. | 稀释Na2CO3溶液时,$\frac{c(HC{{O}_{3}}^{-}•c(O{H}^{-}))}{c(C{{O}_{3}}^{2-})}$增大 | |
| B. | 常温下,反应4Fe(OH)2(s)+2H2O(I)+O2(g)═4Fe(OH)3(s)的△H<0,△S<0 | |
| C. | 用0.1mol•L-1CH3COOH溶液滴定0.1mol•L-1 NaOH至中性时:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小 |
3.下列说法正确的是( )
| A. | 苯分子可表示为 ,其邻二氯代物有2种结构 ,其邻二氯代物有2种结构 | |
| B. | 等物质的量C2H4、C3H6完全燃烧,消耗等质量的O2 | |
| C. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 | |
| D. | 利用CH4和Cl2的取代反应可制取溶剂CCl4 |
20.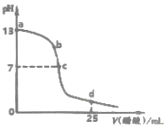 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )| A. | a~c区间内(不包含a、c两点)可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | c点时溶液中:c(Na+)=c(CH3COO-) | |
| C. | d点时溶液中:c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.2000mol•L-1 | |
| D. | 反应过程中溶液中阴、阳离子总数:b点小于c点 |
1.下列关于有机物的说法正确的是( )
| A. | 有机物只能存在于动植物体内,不能通过人工的方法合成 | |
| B. | 有机物只含有碳、氢两种元素 | |
| C. | 含碳元素的化合物不一定属于有机物 | |
| D. | 烃是指燃烧后只生成CO2和H2O的有机物 |

 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl;
+HCl; .
. 的同分异构体有多种,其中满足下列条件的同分异构体有6种,其中苯环上的一氯代物有两种的同分异构体的结构简式为
的同分异构体有多种,其中满足下列条件的同分异构体有6种,其中苯环上的一氯代物有两种的同分异构体的结构简式为 、
、 .
.