题目内容
8.25℃时,PH=11的NaOH溶液和NaCN溶液中,由水电离出的c(OH-)的关系( )| A. | 相等 | B. | 后者是前者的11倍 | ||
| C. | 后者是前者的108 | D. | 前者是后者的108 |
分析 酸或碱抑制水电离,含有弱根离子的盐促进水电离,根据溶液的pH结合水的离子积常数计算水电离出的氢氧根离子浓度.
解答 解:氢氧化钠抑制水电离,氢氧化钠溶液中水电离出的氢氧根离子浓度等于氢离子浓度,则氢氧化钠溶液中水电离出的c(OH-)=c(H+)=10-11mol/L;氰化钠是强碱弱酸盐,促进水电离,溶液中氢氧根离子就是水电离出的氢氧根离子,所以由水电离出的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-11}}$mol/L=0.001mol/L,则由水电离出的c(OH-)之比=10-11mol/L:0.001mol/L=10-8:1,故选C.
点评 本题考查了pH的简单计算,明确酸或碱、含有弱根离子的盐对水电离的影响是解本题关键,难度中等.

练习册系列答案
相关题目
1. 氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g);△H<0.
氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g);△H<0.
(1)在373K时,向2L的密闭容器中通入SO2、SCl2与Cl2均为0.04mol,发生上述反应.测得其压强(p)随时间(t)的变化为表中数据I(反应达到平衡时的温度与起始温度相同).
请回答下列问题:
①反应开始至达到平衡时,v(SOCl2)=0.005mol/(L•min).
②若只改变某一条件,其他条件相同时,测得其压强随时间的变化为表中数据II,则改变的条件是使用催化剂.
(2)如图是某同学测定上述反应的平衡常数的对数值(lgK)与温度的变化关系点.
①A点的数值为2.6.(已知:lg4=0.6)
②当升高到某一温度时,反应重新达到平衡,A点可能变化为B、E点.
(3)已知反应S4(g)+4Cl2(g)═4SCl2(g)的△H=-4kJ•mol-1,1molS4(g)、1molSCl2(g)分子中化学键断裂时分别需要吸收1064kJ、510kJ的能量,则1molCl2(g)分子中化学键断裂时需吸收的能量为243kJ.
(4)某种锂电池的负极由金属锂构成,正极由二氯亚砜(SOCl2)和碳材料构成.总反应为:4Li+2SOCl2═4LiCl+S+SO2↑,此种锂电池是一次电池,在放电时有气体产生.此电池工作时正极的电极反应式为2SOCl2+4e-=S+SO2↑+4Cl-,电解质中锂离子移向正极(填“正极”或“负极”).
 氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g);△H<0.
氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g);△H<0.(1)在373K时,向2L的密闭容器中通入SO2、SCl2与Cl2均为0.04mol,发生上述反应.测得其压强(p)随时间(t)的变化为表中数据I(反应达到平衡时的温度与起始温度相同).
| t/min | 0 | 1 | 2 | 3 | 4 | 5 | |
| I | p | 6.0p0 | 6.7p0 | 6.1p0 | 5.4p0 | 5.0p0 | 5.0p0 |
| II | p | 6.0p0 | 7.0p0 | 5.3p0 | 5.0p0 | 5.0p0 | 5.0p0 |
①反应开始至达到平衡时,v(SOCl2)=0.005mol/(L•min).
②若只改变某一条件,其他条件相同时,测得其压强随时间的变化为表中数据II,则改变的条件是使用催化剂.
(2)如图是某同学测定上述反应的平衡常数的对数值(lgK)与温度的变化关系点.
①A点的数值为2.6.(已知:lg4=0.6)
②当升高到某一温度时,反应重新达到平衡,A点可能变化为B、E点.
(3)已知反应S4(g)+4Cl2(g)═4SCl2(g)的△H=-4kJ•mol-1,1molS4(g)、1molSCl2(g)分子中化学键断裂时分别需要吸收1064kJ、510kJ的能量,则1molCl2(g)分子中化学键断裂时需吸收的能量为243kJ.
(4)某种锂电池的负极由金属锂构成,正极由二氯亚砜(SOCl2)和碳材料构成.总反应为:4Li+2SOCl2═4LiCl+S+SO2↑,此种锂电池是一次电池,在放电时有气体产生.此电池工作时正极的电极反应式为2SOCl2+4e-=S+SO2↑+4Cl-,电解质中锂离子移向正极(填“正极”或“负极”).
17.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是A(填写物质的序号).
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)为配制500mL上述“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管.(在横线上填写相应仪器的名称),
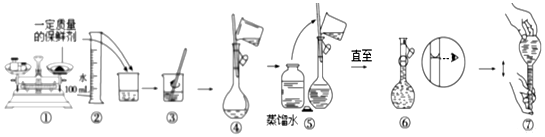
(3)某同学取用保鲜剂固体配制溶液的过程如图所示,其错误操作序号是①⑤
(4)在溶液配制过程中,下列实验操作会使配得的溶液浓度偏大的是AC.
A.溶解固体时,未冷却就直接转移
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)为配制500mL上述“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管.(在横线上填写相应仪器的名称),
(3)某同学取用保鲜剂固体配制溶液的过程如图所示,其错误操作序号是①⑤

(4)在溶液配制过程中,下列实验操作会使配得的溶液浓度偏大的是AC.
A.溶解固体时,未冷却就直接转移
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度.