题目内容
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲,D的L层电子数等于K、M两个电子层上的电子数之和.
(1)写出下列元素的化学式:A ,B ,C ,D ;
(2)D的质子数和中子数相等,D的原子组层符号为 ,它的最高价为 价,它的电子排布图是 .
(3)AD2的空间构型是 ,写出C2B2的电子式 ;
(4)氢元素与B、D均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是 .
(1)写出下列元素的化学式:A
(2)D的质子数和中子数相等,D的原子组层符号为
(3)AD2的空间构型是
(4)氢元素与B、D均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,据此解答.
解答:
解:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,
(1)由上述分析可知,A为C元素、B为O元素、C为Na元素、D为S元素,故答案为:C;O;Na;S;
(2)D为S元素,D的质子数和中子数相等,D的原子组层符号为
S,最高价化合价等于最外层电子数6,核外电子排布图为: ,故答案为:
,故答案为:
S;+6; ;
;
(3)AD2为CS2,与二氧化碳等电子体,空间构型是直线型,C2B2为Na2O2,电子式是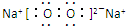 ,故答案为:直线型;
,故答案为:直线型;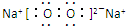 ;
;
(4)氢元素与B、D均可以形成原子个数比为2:1的化合物,分别是硫化氢和水,水分子与分子之间存在氢键,所以水的熔沸点高于硫化氢,
故答案为:水分子与分子之间存在氢键.
(1)由上述分析可知,A为C元素、B为O元素、C为Na元素、D为S元素,故答案为:C;O;Na;S;
(2)D为S元素,D的质子数和中子数相等,D的原子组层符号为
16 8 |
 ,故答案为:
,故答案为:16 8 |
 ;
;(3)AD2为CS2,与二氧化碳等电子体,空间构型是直线型,C2B2为Na2O2,电子式是
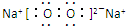 ,故答案为:直线型;
,故答案为:直线型;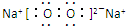 ;
;(4)氢元素与B、D均可以形成原子个数比为2:1的化合物,分别是硫化氢和水,水分子与分子之间存在氢键,所以水的熔沸点高于硫化氢,
故答案为:水分子与分子之间存在氢键.
点评:本题考查结构性质位置关系应用,侧重对化学用语的考查,比较基础,注意对基础知识的积累掌握.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
有关化学用语正确的是( )
A、Be原子的结构示意图  |
| B、乙醇的结构简式:C2H5OH |
| C、明矾的化学式KAlSO4?12H2O |
| D、乙烯的结构式:CH2=CH2 |
下列各组反应中最终肯定是白色沉淀的是( )
| A、AlCl3溶液中加入过量氨水 |
| B、Al2(SO4)3溶液中加入过量KOH溶液 |
| C、FeCl2溶液中加入过量氨水 |
| D、Ca(OH)2溶液中通入过量SO2气体 |
 向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是( )
向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是( )| A、在a点对应的溶液中,加入Mg2+、I-、NH4+、NO3-离子仍能大量共存 |
| B、原溶液中盐酸和AlCl3物质的量的浓度之比为1:3 |
| C、若b、c的纵坐标数值相同,则横坐标数值之比为1:3 |
| D、图中B→C的过程中,实际发生的离子方程式为Al(OH)3+OH-=AlO2-+2H2O |
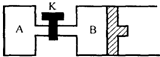 如图所示,B中活塞可以自由滑动.A、B中均有1mol X、1mol Y,起始时,V(A)=V(B)=a L.关闭K,相同温度下,两容器中同时发生反应:2X(g)+2Y(g)=Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8a L.
如图所示,B中活塞可以自由滑动.A、B中均有1mol X、1mol Y,起始时,V(A)=V(B)=a L.关闭K,相同温度下,两容器中同时发生反应:2X(g)+2Y(g)=Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8a L.