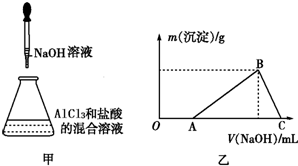
题目内容
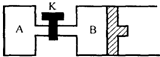 如图所示,B中活塞可以自由滑动.A、B中均有1mol X、1mol Y,起始时,V(A)=V(B)=a L.关闭K,相同温度下,两容器中同时发生反应:2X(g)+2Y(g)=Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8a L.
如图所示,B中活塞可以自由滑动.A、B中均有1mol X、1mol Y,起始时,V(A)=V(B)=a L.关闭K,相同温度下,两容器中同时发生反应:2X(g)+2Y(g)=Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8a L.(1)达到平衡所需的时间:A
(2)W的百分含量:A
(3)B中X的转化率为
(4)打开K,重新达平衡(Ⅱ)时,B的体积为
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)由于该反应是体积减小的反应,所以在反应过程中A容器中的压强小于B容器,根据压强对反应速率的影响判断;
(2)达到平衡后B容器中压强大于A容器中的,根据压强对平衡移动的影响判断;
(3)根据转化率=
×100%计算;
(4)利用等效平衡的思想答题;
(2)达到平衡后B容器中压强大于A容器中的,根据压强对平衡移动的影响判断;
(3)根据转化率=
| 转化的气体体积 |
| 起始气体体积 |
(4)利用等效平衡的思想答题;
解答:
解:(1)由于该反应是体积减小的反应,则B中的活塞可以移动,所以在反应过程中A容器中的压强小于B容器,所以B中反应的速率大于A容器中的,反应所需时间少,故答案为:>;
(2)反应开始后直到达到平衡,B容器中压强都大于A容器中的,所以B容器中反应正向进行的程度大于A容器,所以W的百分含量:A<B,故答案为:<;
(3)当V(B)=0.8aL,B的体积减小了0.2aL,则消耗了0.4aL的X,因为原来有0.5aL的X,所以转化率=
×100%=80%,故答案为:80%;
(4)当打开K后,A将达到与未打开K时的B同样的平衡,即为等效平衡,体积将减少0.2aL,A、B气体体积之和为1.6aL,所以此时B的体积为1.6aL-aL=0.6aL,故答案为:0.6a;
(2)反应开始后直到达到平衡,B容器中压强都大于A容器中的,所以B容器中反应正向进行的程度大于A容器,所以W的百分含量:A<B,故答案为:<;
(3)当V(B)=0.8aL,B的体积减小了0.2aL,则消耗了0.4aL的X,因为原来有0.5aL的X,所以转化率=
| 0.4a |
| 0.5a |
(4)当打开K后,A将达到与未打开K时的B同样的平衡,即为等效平衡,体积将减少0.2aL,A、B气体体积之和为1.6aL,所以此时B的体积为1.6aL-aL=0.6aL,故答案为:0.6a;
点评:本题主要考查了恒容和恒压条件下平衡的移动及计算,中等难度,解题时注意两个容器在瓜过程中压强的关系.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、葡萄糖注射液不能产生丁达尔效应,不属于胶体 |
| B、可用蘸浓盐酸的棉棒检验输送氨气的管道是平否漏气 |
| C、明矾和漂白粉常用于自来水的净化和杀菌流消毒,两者原理相同 |
| D、化学变化中一定有能量变化,而有能量变化过程不一定发生化学反应 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、氧化镁、氧化铝的熔点都很高,都可用作耐高温材料 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、品红溶液通入二氧化硫,品红褪色,再加热不恢复红色 |
| D、锌的金属活泼性比铁强,可在海轮外壳上装若干锌块以减缓其腐蚀 |
某烃通式为CnH2n,该烃可能为( )
| A、丙烷 | B、丙烯 | C、丙炔 | D、苯 |
下列说法中不正确的是( )
| A、Na2O2可做呼吸面具的供氧剂 |
| B、单质硅是生产光导纤维的基本原料 |
| C、目前世界上使用量最大的合金是钢 |
| D、明矾可作净水剂 |