题目内容
6.X、Y、Z、W是原子序数依次增大的短周期主族元素,X与Z同主族,X原子的最外层电子数是其电子数的$\frac{2}{3}$,Y和W是同一周期中原子半径相差最大两种元素.下列叙述正确的是( )| A. | 原子半径:W>Z | |
| B. | X、Y 均能与W形成的离子化合物 | |
| C. | Z、W的气态氢化物的稳定性:Z>W | |
| D. | X、Z的最高价氧化物的水化物酸性:X>Z |
分析 X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子的最外层电子数是其电子数的$\frac{2}{3}$,最外层最多含有8个电子,则X核外含有6个电子,最外层含有4个电子,为C元素;X与Z同主族,则Z为Si元素;Y和W是同一周期中原子半径相差最大两种元素,则Y、W都位于第三周期,Y为Na元素、W为Cl元素,据此结合元素周期律知识解答.
解答 解:X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子的最外层电子数是其电子数的$\frac{2}{3}$,最外层最多含有8个电子,则X核外含有6个电子,最外层含有4个电子,为C元素;X与Z同主族,则Z为Si元素;Y和W是同一周期中原子半径相差最大两种元素,则Y、W都位于第三周期,Y为Na元素、W为Cl元素,
A.Z为Si元素、W为Cl元素,二者位于同一周期,原子序数越大原子半径越小,则原子半径Z>Si,即W<Z,故A错误;
B.X、Y、W分别为C、Na、Cl元素,C、Cl元素只能形成共价化合物,故B错误;
C.非金属性越强,对应氢化物的稳定性越强,非金属性Z<W,二者气态氢化物的稳定性:Z<W,故C错误;
D.X、Z分别为C、Si,非金属性C>Si,则最高价氧化物的水化物酸性:X>Z,故D正确;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
11.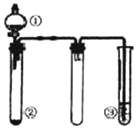 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
| B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
| C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
| D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
| A. | A | B. | B | C. | C | D. | D |
12.下列叙述正确的是( )
| A. | K+、ClO‐、SO42‐、HCO3‐一定能共存于 c(Fe3+)=0.1mol•L‐l 的溶液中 | |
| B. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 在NaClO和NaCl混合溶液中滴入过量SO2气体,反应的离子方程式为:SO2+3C1O‐+H2O═SO42‐+C1‐+2HClO | |
| D. | Na+、HCO3-、Br-、Mg2+可以在 pH=8 的溶液中共存 |
14.跟12.8gSO2所含原子数相等的NO的质量为( )
| A. | 3.0g | B. | 6.0g | C. | 9.0g | D. | 18.0g |
11.下列说法符合事实的是( )
| A. | 常温下,加入铝粉能够产生氢气的溶液中水电离的c(H+)一定小于10-7mol•L-1 | |
| B. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.在含Cl-、CrO42-浓度相同的溶液中滴加稀AgNO3溶液时,先生成Ag2CrO4沉淀 | |
| C. | 温度一定时,强电解质溶液的导电能力一定比弱电解质溶液强 | |
| D. | 实验室用锌制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
15.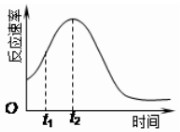 某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
(1)猜想Ⅱ可能是:生成的Mn2+在反应中起到催化剂的作用,加快了反应速率
(2)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
 某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
(1)猜想Ⅱ可能是:生成的Mn2+在反应中起到催化剂的作用,加快了反应速率
(2)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | 2mL0.1mol/L H2C2O4溶液、1mL 0.05mol/L 酸性KMnO4 | 2mL0.1mol/L H2C2O4溶液、1mL 0.05mol/L 酸性KMnO4,少量MnSO4(s)固体(填物质名称) |
| 实验现象(褪色时间) | 褪色时间10min | 褪色时间<10min(选填“<”“>”或“=”) |
| 结论 | 猜想Ⅱ正确 | |
16.已知自然界氧的同位素有16O、17O、18O,与氢的其中两种同位素H、D组成水分子,从水分子的原子组成来看,此水一共有( )
| A. | 3种 | B. | 18种 | C. | 9种 | D. | 12种 |
 A元素最简单的氢化物的电子式为
A元素最简单的氢化物的电子式为 .
.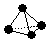 ,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:N4(g)=2N2(g)△H=-882kJ•mol-1;
,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:N4(g)=2N2(g)△H=-882kJ•mol-1;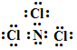 ;X遇水蒸气可形成一种常见的漂白性物质.则X与水反应的化学方程式是NCl3+3H2O=NH3↑+3HClO.
;X遇水蒸气可形成一种常见的漂白性物质.则X与水反应的化学方程式是NCl3+3H2O=NH3↑+3HClO.