题目内容
3.电解降解法可用于治理水体硝酸盐污染,将NO3-降解成N2的电解装置如图所示.下列说法正确的是(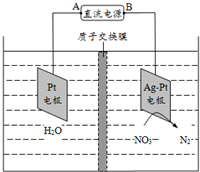
| A. | 电源的正极为b | |
| B. | 电解时H+从膜右侧迁移到膜左侧 | |
| C. | Ag-Pt电极反应为:2H2O-4e-=4H++O2↑ | |
| D. | 若转移的电子数为1.204×1024,生成N25.6 g |
分析 根据图象知,硝酸根离子得电子发生还原反应,则Ag-Pt作阴极,Pt电极为阳极,
A.与电源负极相连的为阴极,与电源正极相连的为阳极;
B.氢离子为阳离子,应移向电解池的阴极;
C.Ag-Pt作阴极,阳离子氢离子在阴极得到电子发生还原反应;
D.依据2NO3-~N2↑~10e-,计算生成氮气的质量.
解答 解:根据图象知,硝酸根离子得电子发生还原反应,则Ag-Pt作阴极,Pt电极为阳极,
A.Ag-Pt作阴极,与电源的负极相连,所以b为负极,故A错误;
B.电解时H+移向电解池的阴极,从膜左侧迁移到膜右侧,故B错误;
C.阴极上是阳离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,故C错误;
D.转移的电子数为1.204×1024,物质的量为2mol,依据2NO3-~N2↑~10e-,可知生成氮气的质量为5.6g,故D正确;
故选D.
点评 本题考查了电解池,熟悉电解池工作原理,准确判断电极及发生的电极反应是解题关键,题目难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
13.某元素最高正价氧化物对应的水化物的化学式是HnXOm,该元素的气态氢化物的化学式为( )
| A. | HnX | B. | H(2m-n)X | C. | H(8+n-2m) X | D. | H(8+2m-n) X |
14.下列物质中,属于共价化合物的是( )
| A. | NH4Cl | B. | SO2 | C. | Cl2 | D. | Na2SO4 |
11.下列各组物质中的四种物质,用一种试剂即可鉴别的是( )
| A. | 苯酚、乙醇、苯、四氯化碳 | B. | 乙烯、乙烷、乙炔、丙烯 | ||
| C. | 甲酸、乙醛、甲酸钠溶液、乙酸乙酯 | D. | 苯乙烯、苯酚、乙苯、甲苯 |
7.对于某一已经建立平衡的可逆反应,当条件改变或采取某项措施时使平衡向正反应方向移动,以下叙述中正确的是( )
①生成物的质量分数一定增大
②生成物的产量一定增加
③反应物的转化率一定增大
④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率
⑥一定使用催化剂.
①生成物的质量分数一定增大
②生成物的产量一定增加
③反应物的转化率一定增大
④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率
⑥一定使用催化剂.
| A. | ①②③ | B. | ②④⑤ | C. | ③④⑤ | D. | ②⑤ |
5.标准状况下,将NO2和O2按4:1体积比充满一烧瓶,烧瓶倒置于水中待液面稳定(假设溶质不向外扩散),则烧瓶内溶液的物质的量浓度为(mol/L)( )
| A. | 1 | B. | 0.8 | C. | $\frac{1}{22.4}$ | D. | $\frac{1}{28}$ |