题目内容
5.标准状况下,将NO2和O2按4:1体积比充满一烧瓶,烧瓶倒置于水中待液面稳定(假设溶质不向外扩散),则烧瓶内溶液的物质的量浓度为(mol/L)( )| A. | 1 | B. | 0.8 | C. | $\frac{1}{22.4}$ | D. | $\frac{1}{28}$ |
分析 NO2和O2按体积比4:1混合后充入一干燥烧瓶中,把烧瓶倒置于水中发生:4NO2+O2+2H2O=4HNO3,根据方程式计算.
解答 解:设混合气体中含有4VLNO2,1VLO2,则烧瓶的体积为5VL,
4NO2+O2+2H2O=4HNO3
$\frac{4V}{22.4}$mol $\frac{V}{22.4}$mol $\frac{V}{22.4}$mol
c(HNO3)=$\frac{\frac{4V}{22.4}mol}{5VL}$=$\frac{4}{5}$×$\frac{1}{22.4}$mol/L=$\frac{1}{28}$mol/L.
故选D.
点评 本题考查物质的量浓度的计算,题目难度不大,注意根据反应的化学方程式计算,把握物质的量的相关计算公式的运用.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
3.电解降解法可用于治理水体硝酸盐污染,将NO3-降解成N2的电解装置如图所示.下列说法正确的是( 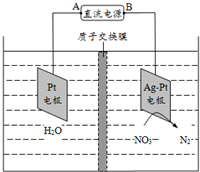

| A. | 电源的正极为b | |
| B. | 电解时H+从膜右侧迁移到膜左侧 | |
| C. | Ag-Pt电极反应为:2H2O-4e-=4H++O2↑ | |
| D. | 若转移的电子数为1.204×1024,生成N25.6 g |
16.含硫48%的硫铁矿煅烧时FeS2损失率为2%,则下列说法不正确的是( )
| A. | 该硫铁矿含FeS2也是48% | B. | 硫损失也是2% | ||
| C. | 铁损失也是2% | D. | 该硫铁矿含铁42% |
10.下列说法中,正确的是( )
| A. | 原子是化学变化中的最小微粒 | |
| B. | 分子是化学变化中的最小微粒 | |
| C. | 原子是可分成更小粒子的实心球 | |
| D. | 原子是构成一切物质的基本粒子,是构成物质的最小粒子 |
14.区别乙醛、苯、溴最好选用的是( )
| A. | 水 | B. | 烧碱溶液 | C. | AgNO3溶液 | D. | 新制Cu(OH)2 |