题目内容
7.对于某一已经建立平衡的可逆反应,当条件改变或采取某项措施时使平衡向正反应方向移动,以下叙述中正确的是( )①生成物的质量分数一定增大
②生成物的产量一定增加
③反应物的转化率一定增大
④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率
⑥一定使用催化剂.
| A. | ①②③ | B. | ②④⑤ | C. | ③④⑤ | D. | ②⑤ |
分析 ①生成物质量增大小于混合物总质量增大,生成物的质量分数可能降低;
②平衡向正反应方向移动,生成物的产量一定增加;
③增大某一反应的浓度,平衡向正反应移动,其它反应物的转化率增大,自身转化率降低;
④如增大反应物的浓度,平衡向正方向移动,达到平衡时,反应物的浓度比改变条件前大;
⑤平衡向正反应移动,正反应速率一定大于逆反应速率;
⑥加入催化剂,正逆反应速率同等程度增大,平衡不移动.
解答 解:①生成物质量增大小于混合物总质量增大,生成物的质量分数可能降低,故①错误;
②平衡向正反应方向移动,生成物的产量一定增加,故②正确;
③增大某一反应的浓度,平衡向正反应移动,其它反应物的转化率增大,自身转化率降低,故③错误;
④如增大反应物的浓度,平衡向正方向移动,达到平衡时,反应物的浓度比改变条件前大,故④错误;
⑤平衡向正反应移动,正反应速率一定大于逆反应速率,故⑤正确;
⑥加入催化剂,正逆反应速率同等程度增大,平衡不移动,故⑥错误;
综上所述②⑤正确,
故选D.
点评 本题考查化学平衡的影响因素,题目难度中等,注意影响化学平衡移动的因素,解答时注意从勒沙特列原理的角度分析.

练习册系列答案
相关题目
5.某温度下,某反应达到平衡,平衡常数k=C(CO2).C(H2)/C(CO).C(H2O).恒容时,升高温度,CO浓度增大.下列说法正确的是( )
| A. | 升高温度,逆反应速率增大,正反应速率减小 | |
| B. | 恒温时,增大压强,CO浓度不变 | |
| C. | 该反应的化学方程式为:CO2+H2?CO+H2O | |
| D. | 该反应的焓变为负值 |
3.电解降解法可用于治理水体硝酸盐污染,将NO3-降解成N2的电解装置如图所示.下列说法正确的是( 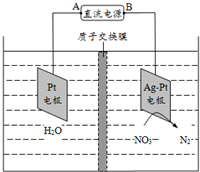

| A. | 电源的正极为b | |
| B. | 电解时H+从膜右侧迁移到膜左侧 | |
| C. | Ag-Pt电极反应为:2H2O-4e-=4H++O2↑ | |
| D. | 若转移的电子数为1.204×1024,生成N25.6 g |
2.已知H2?C3H8的燃烧热分别为285.8kJ•mol-1和2220.0kJ•mol-1,实验测得H2和C3H8的混合气体共5mol,完全燃烧时放热3847kJ,则混合气体中H2和C3H8的体积约为( )
| A. | 1:3 | B. | 3:1 | C. | 1:4 | D. | 5:13 |
12.在氧化还原反应中,下列叙述正确的是( )
| A. | 物质失电子的反应为氧化反应 | |
| B. | 物质在变化中失去了电子,此物质是氧化剂 | |
| C. | 发生电子转移的反应即是氧化还原反应 | |
| D. | 发生化合价升降的反应不一定是氧化还原反应 |
19.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:r(A)>r(B)>r(D)>r(C) | B. | 离子半径:r(C3-)>r(D-)>r(B+)>r(A2+) | ||
| C. | 原子序数:d>c>b>a | D. | 单质的还原性:A>B>D>C |
16.含硫48%的硫铁矿煅烧时FeS2损失率为2%,则下列说法不正确的是( )
| A. | 该硫铁矿含FeS2也是48% | B. | 硫损失也是2% | ||
| C. | 铁损失也是2% | D. | 该硫铁矿含铁42% |
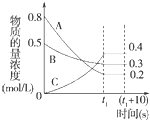 在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题:
在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题: 2C.
2C.