题目内容
18.一元醇A中氧的质量分数约为21.6%.则A的分子式为C4H10O.分析 一元醇A分子中含有1个O原子,根据A分子中质量分数约为21.6%可计算出A的相对分子量,再利用商余法确定其分子式,由此分析解答.
解答 解:一元醇A中氧的质量分数约为21.6%,该醇的相对分子量为:$\frac{16}{21.6%}$=74,
A分子中C、H总原子量为:74-16=58,
根据商余法可得:$\frac{58}{14}$=4…2,
所以A的分子式为:C4H10O,故答案为:C4H10O.
点评 本题考查了有机物分子式、结构式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握商余法、质量守恒定律在确定有机物分子式中的应用方法.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
19.下列关于实验的说法正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 分离Fe(OH)3胶体和FeCl3溶液 | 将混合液倒入过滤器中过滤 |
| B | 证明Ksp(CuS)<Ksp(ZnS) | 向10mL0.1mol/LNa2S溶液中滴入几滴0.1mol/L ZnCl2溶液,产生白色沉淀,再加入CuSO4溶液,产生黑色沉淀 |
| C | 证明酸性:H2CO3>H3BO3 | 向Na2CO3中滴入过量H3BO3溶液,无气泡冒出 |
| D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没,产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
9.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1mol CO2、CO的混合气中含有的碳原子数为NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 1mol氯气与足量的氢氧化钠溶液完全反应转移的电子数为2NA | |
| D. | 1L 1mol•L-1 CuCl2溶液中含有的氯离子数为NA |
6.下列关于化工生产原理的叙述中,符合当前工业生产实际的是( )
| A. | 氯碱工业中,氢氧化钠在电解槽的阳极区产生 | |
| B. | 硫酸工业中,二氧化硫催化氧化使用催化剂,可增加二氧化硫的转化率 | |
| C. | 合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 | |
| D. | 接触法制硫酸中三氧化硫用水吸收制成浓硫酸 |
3.设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 100mL0.4mol/L的甲酸中含甲酸的分子数为0.04NA | |
| B. | 在标准状态下,22.4L乙烷与乙烯的混合气体,含碳原子数为2NA | |
| C. | 18g水中含有的电子数为10NA | |
| D. | NA个23Na原子的质量为23g |
10.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol甲基中含有电子数为10NA | |
| B. | 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA | |
| C. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA | |
| D. | 50mL12mol•L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA |
7.化学与生活、社会可持续发展密切相关,下列叙述错误的是( )
| A. | CO2的大量排放会导致酸雨的形成 | |
| B. | 黄河三角洲的形成体现了胶体聚沉的性质 | |
| C. | 推广使用燃料电池汽车,可减少颗粒物、CO等有害物质的排放 | |
| D. | 轮船上挂锌锭防止铁腐蚀,属于牺牲阳极的阴极保护法 |
8.食用二氧化硫漂白过的食品,对人体的肝、肾脏等有严重损害.某科研小组设计实验检验二氧化硫的漂白性.回答下列问题:
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.
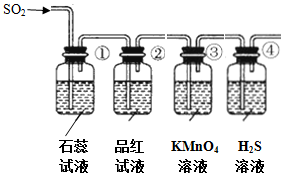
(2)根据上述实验,回答下列问题:
(3)用SO2漂白过的食品中一般残留有亚硫酸盐,科研小组设计了检验食品中是否含有亚硫酸盐的简单方法:将食品剪成碎末放入烧杯,加入适量的水,加热一会儿,冷却至室温,滴加盐酸和试剂A,观察液体的颜色变化既可.
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.

(2)根据上述实验,回答下列问题:
| 序号 | 实验现象 | 解释原因 |
| ① | 石蕊试液变红 | 石蕊试液变红说明SO2是酸性气体 |
| ② | 品红试液褪色 | SO2具有漂白性 |
| ③ | KMnO4溶液颜色褪色 | 反应的离子方程式5SO2+2H2O+2MnO4-=2Mn2++5SO42-+4H+ |
| ④ | 溶液变浑浊,有黄色沉淀生成 | SO2+2H2S=3S↓+2H2O |
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.