题目内容
9.用NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 标准状况下,1mol CO2、CO的混合气中含有的碳原子数为NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 1mol氯气与足量的氢氧化钠溶液完全反应转移的电子数为2NA | |
| D. | 1L 1mol•L-1 CuCl2溶液中含有的氯离子数为NA |
分析 A.二氧化碳和CO中均含1个碳原子;
B.标准状况下气体摩尔体积为22.4L/mol;
C.氯气和氢氧化钠溶液反应发生的是自身氧化还原反应,氯元素化合价从0价变化为+1价和-1价;
D.溶液中离子物质的量=溶质物质的量×离子数.
解答 解:A.二氧化碳和CO中均含1个碳原子,故1mol二氧化碳和CO中含有的碳原子的物质的量为1mol,个数为NA个,故A正确;
B.常温常压下,11.2L氯化氢气体物质的量不是0.5mol,故B错误;
C.氯气和氢氧化钠溶液反应发生的是自身氧化还原反应,氯元素化合价从0价变化为+1价和-1价,1mol氯气与足量的氢氧化钠溶液完全反应转移的电子数为NA,故C错误;
D.1L 1mol•L-1 CuCl2溶液中含有的氯离子数=1L×1mol•L-1×2×NA =2NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的条件应用,氧化还原反应电子转移计算,溶液中溶质微粒数的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
10.下列仪器为冷凝管的是( )
| A. |  | B. |  | C. | 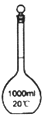 | D. | 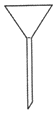 |
11.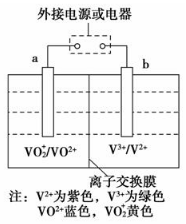 某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
 某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )
某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性.充电时右槽溶液颜色由绿色变为紫色.下列叙述正确的是( )| A. | 放电时,H+从左槽迁移进右槽 | |
| B. | 放电过程中,左槽溶液颜色由黄色变为蓝色 | |
| C. | 充电时,b极接直流电源正极,a极接直流电源负极 | |
| D. | 充电过程中,a极的电极反应式为:VO2++2H++e-═VO2++H2O |
17.以下配制溶液叙述正确的是( )
| A. | 配制一定物质的量浓度溶液时,若加水超容最瓶刻度应用胶头滴管将多余溶液吸出 | |
| B. | 用容量瓶配制溶液,定容时俯视读数,所配溶液浓度偏大 | |
| C. | 欲配制1L1.0mol/L的NaCl溶液,可将58.5gNaCl溶于IL水中 | |
| D. | 稀释后的H2SO4未等冷却至室温可立即转移到容最瓶中 |
4.下列说法中正确的是( )
| A. | 分子间作用力越大,分子越稳定 | |
| B. | 分子间作用力越大,物质的熔、沸点越高 | |
| C. | 相对分子质量越大,其分子间作用力越大 | |
| D. | 分子间只存在范德华力 |
1.下列大小关系中不正确的是( )
| A. | 沸点:正己烷>3-甲基戊烷>2-甲基丁烷 | |
| B. | 含氢量:乙烯>乙苯>乙炔 | |
| C. | 密度:苯>H2O>CCl4 | |
| D. | 相同质量的物质含共用电子对总数:乙烷>乙烯>乙炔 |
19.某晶体化学式为N2H6SO4,其晶体类型与硫酸铵相同.试分析在该晶体中不会存在( )
| A. | 阳离子 | B. | 共价键 | C. | 离子键 | D. | 分子间作用力 |