题目内容
铝用作焊接钢轨是利用( )
| A、铝同氧气反应生成稳定的保护层 |
| B、铝是热的良导体 |
| C、铝合金强度大 |
| D、铝是强还原剂,铝热反应放热 |
考点:铝的化学性质
专题:
分析:高温条件下,铝和氧化铁发生置换反应生成铁单质同时放出大量热,从而用于焊接钢轨,据此分析解答.
解答:
解:高温条件下,铝和氧化铁发生置换反应生成铁单质同时放出大量热而使铁熔融为铁水,从而用于焊接钢轨,铝用作焊接钢轨是利用铝的还原性及铝热反应放出的热,与铝合金硬度、铝的导电性及铝同氧气反应生成稳定的保护层无关,
故选D.
故选D.
点评:本题以铝热反应为载体考查铝的性质,明确铝热反应原理是解本题关键,会正确书写方程式,题目难度不大.

练习册系列答案
相关题目
下列解释事实或实验现象的离子方程式不正确的是( )
| A、用食醋除去暖水瓶中的水垢,水垢溶解,有无色气泡产生:2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O |
| B、用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O |
| C、向NaHCO3和CaCl2混合溶液中,加入少量NaOH溶液:OH-+HCO32-═CO32-+H2O |
| D、用小苏打治疗胃酸过多:HCO3-+H+═H2O+CO2↑ |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、由水电离的c(OH-)=10-12mol?L-1的溶液中:Br-、CO32-、K+、SO32- |
| B、含有大量AlO2-的溶液中:K+、Fe3+、Br-、SO42- |
| C、和Al反应放出氢气的溶液:Na+、Cl-、NH4+、NO3- |
| D、使pH试纸变深蓝色的溶液中:Cl-、K+、Mg2+、SO42- |
已知A为常见的金属单质,根据如图所示的转化关系回答下列问题.

(1)确定A、B、C、D、E、F的化学式:
A为 ,B为 ,C为 .
D为 ,E为 ,F为 .
(2)写出⑧的化学方程式及④、⑤的离子方程式: .

(1)确定A、B、C、D、E、F的化学式:
A为
D为
(2)写出⑧的化学方程式及④、⑤的离子方程式:
下列说法正确的是( )
| A、碳酸氢钠的热稳定性小于碳酸钠的 |
| B、Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
| C、可用石灰水区分Na2CO3与NaHCO3溶液 |
| D、滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 |

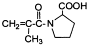 有多种同分异构体,如
有多种同分异构体,如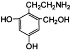 等.写出其中满足下列条件的同分异构体:A.含有苯环,不含甲基;B.能与NaOH溶液以物质的量之比1:1完全中和;C.苯环上一卤代物只有一种,
等.写出其中满足下列条件的同分异构体:A.含有苯环,不含甲基;B.能与NaOH溶液以物质的量之比1:1完全中和;C.苯环上一卤代物只有一种,
 (1)下列实验操作中,错误的是
(1)下列实验操作中,错误的是